题目内容
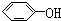
17.某有机物甲和A互为同分异构体,经测定它们的相对分子质量小于100;将1mol甲在O2中充分燃烧得到等物质的量的CO2和H2O (g ),同时消耗112LO2(标准状况);在酸性条件下将1mol甲完全水解可以生成1mol 乙 和1mol丙;而且在一定条件下,丙可以被连续氧化成为乙.(1)请确定并写出甲的分子式C4H8O2;与甲属同类物质的同分异构体共有4种(包含甲).
经红外光谱测定,在甲和A的结构中都存在C=O双键和C-O单键,B在HIO4存在并加热时只生成一种产物C,下列为各相关反应的信息和转化关系:
①ROH+HBr(氢溴酸)$\stackrel{△}{→}$RBr+H2O
②
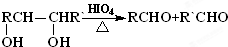

(2)E→F 的反应类型为消去反应;
(3)G 的结构简式为
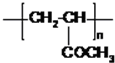 ;
;(4)B→D的反应化学方程式为:
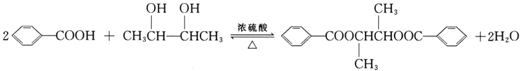 ;
;(5)写出C在条件①下进行反应的化学方程式:
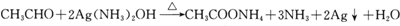 .
.
分析 1mol甲在酸性条件下可水解生成1mol 乙和1mol丙,则甲中含有酯基,且丙通过一定途径可转化为乙,则丙是醇,乙是酸,1mol的某有机物甲在O2中充分燃烧,可得到等体积的CO2和H2O(g ),并消耗112L O2(标准状况),设有机物X的分子式为CnH2nOx,CnH2nOx+O2→nCO2++nH2O,由1mol有机物X完全燃烧需要5molO2知,3n-x=10,且M<100,只有C4H8O2符合题意,则甲是乙酸乙酯,乙是乙酸,丙是乙醇;C和银氨溶液发生银镜反应然后酸化得乙酸,则C是乙醛,A与甲为同分异构体,且A中含有碳氧双键,B只生成C,根据题给信息知,B为CH3CH(OH)CH(OH)CH3,A为CH3COCH(OH)CH3,在浓硫酸作催化剂、加热条件下,CH3CH(OH)CH(OH)CH3和苯甲酸发生酯化反应生成D,则D的结构简式为: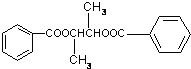 ,A和氢溴酸发生取代反应生成E,则E的结构简式为:CH3COCH(Br)CH3,E和氢氧化钠的醇溶液发生消去反应生成F,则F的结构简式为:CH3COCH=CH2,F在一定条件下发生加聚反应生成G,则G的结构简式为:
,A和氢溴酸发生取代反应生成E,则E的结构简式为:CH3COCH(Br)CH3,E和氢氧化钠的醇溶液发生消去反应生成F,则F的结构简式为:CH3COCH=CH2,F在一定条件下发生加聚反应生成G,则G的结构简式为: .
.
解答 解:1mol甲在酸性条件下可水解生成1mol 乙和1mol丙,则甲中含有酯基,且丙通过一定途径可转化为乙,则丙是醇,乙是酸,1mol的某有机物甲在O2中充分燃烧,可得到等体积的CO2和H2O(g ),并消耗112L O2(标准状况),设有机物X的分子式为CnH2nOx,CnH2nOx+O2→nCO2++nH2O,由1mol有机物X完全燃烧需要5molO2知,3n-x=10,且M<100,只有C4H8O2符合题意,则甲是乙酸乙酯,乙是乙酸,丙是乙醇;C和银氨溶液发生银镜反应然后酸化得乙酸,则C是乙醛,A与甲为同分异构体,且A中含有碳氧双键,B只生成C,根据题给信息知,B为CH3CH(OH)CH(OH)CH3,A为CH3COCH(OH)CH3,在浓硫酸作催化剂、加热条件下,CH3CH(OH)CH(OH)CH3和苯甲酸发生酯化反应生成D,则D的结构简式为: ,A和氢溴酸发生取代反应生成E,则E的结构简式为:CH3COCH(Br)CH3,E和氢氧化钠的醇溶液发生消去反应生成F,则F的结构简式为:CH3COCH=CH2,F在一定条件下发生加聚反应生成G,则G的结构简式为
,A和氢溴酸发生取代反应生成E,则E的结构简式为:CH3COCH(Br)CH3,E和氢氧化钠的醇溶液发生消去反应生成F,则F的结构简式为:CH3COCH=CH2,F在一定条件下发生加聚反应生成G,则G的结构简式为 ,
,
(1)根据上面的分析可知,甲的分子式为C4H8O2,与甲属同类物质的同分异构体有甲酸丙酯、甲酸异丙酯、乙酸乙酯、丙酸甲酯,所以有4种,
故答案为:C4H8O2,4;
(2)E的结构简式为:CH3COCH(Br)CH3,E和氢氧化钠的醇溶液发生消去反应生成F,故答案为:消去;
(3)通过以上分析知,G的结构简式分别为: ,故答案为:
,故答案为: ;
;
(4)在浓硫酸作催化剂、加热条件下,2,3-丁二醇和苯甲酸发生酯化反应,反应方程式为: ,
,
故答案为: ;
;
(5)乙醛和银氨溶液发生银镜反应,反应方程式为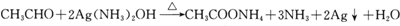 ,
,
故答案为: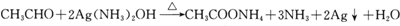 .
.
点评 本题考查有机物的推断,题目难度中等,本题注意把握有机物分子式的确定,推断时注意把握突破口,把握有机物官能团的性质以及转化,特别是题给信息,在解答时要注意审题.

 阅读快车系列答案
阅读快车系列答案| A. | Cu2+、Na+、SO42-、Cl- | B. | K+、Na+、HCO3-、NO3- | ||
| C. | OH-、Cl-、Ca2+、Na+ | D. | Fe2+、Na+、Cl-、NO3- |
| A. | 原子半径:X>Y>Z | B. | 单质的非金属性:X>Y>Z | ||
| C. | 气态氢化物稳定性:X<Y<Z | D. | 原子序数:X>Y>Z |
| A. | 氢 | B. | 钙 | C. | 铁 | D. | 碘 |
| A. | 标准状况下,22.4L SO3所含的分子数目为NA | |
| B. | 0.2molH2O2催化分解,转移电子数为0.2NA | |
| C. | 0.1mol/L的100mLH2SO3溶液中,含有的离子数约为0.03NA | |
| D. | 6.25 mL1 mol/L浓硫酸与足量铜反应,转移电子数为0.2NA |
| A. | 良好的导电性 | B. | 良好的延展性 | C. | 反应中易失电子 | D. | 良好的导热性 |
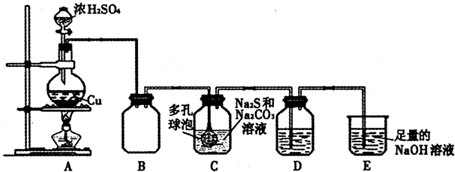
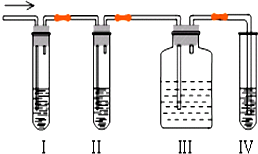 石油裂解产品乙烯是一种重要的化工原料,我们已学过用两种方法制得乙烯:在实验室里用乙醇与浓硫酸共热制乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2,回答下列问题:
石油裂解产品乙烯是一种重要的化工原料,我们已学过用两种方法制得乙烯:在实验室里用乙醇与浓硫酸共热制乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2,回答下列问题: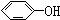 与
与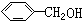
 与
与