题目内容
【题目】氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)写出实验室制备氨气的化学方程式:______________________________ ;氨的水溶液显弱碱性,其原因为__________________________(用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的pH________(填“升高”或“降低”) ;若加入少量的明矾,溶液中的NH的浓度________(填“增大”或“减小”) 。
(2)硝酸铵加热分解可得到N2O和H2O。250 ℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为________________________________,平衡常数表达式为________;若有1 mol硝酸铵完全分解,转移的电子数为________mol。
(3)将pH=12的氨水和pH=2的盐酸等体积混合后溶液呈______性。
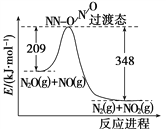
(4)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1 mol N2,其ΔH=________kJ·mol-1。
【答案】 2NH4Cl+Ca(OH)2 ![]() 2NH3+CaCl2+2H2O NH3·H2O
2NH3+CaCl2+2H2O NH3·H2O ![]() NH4++OH- 降低 增大 NH4NO3
NH4++OH- 降低 增大 NH4NO3 ![]() N2O↑+2H2O c(N2O)×c2(H2O) 4 碱 -139
N2O↑+2H2O c(N2O)×c2(H2O) 4 碱 -139
【解析】(1)实验室用氯化铵和氢氧化钙加热反应制备氨气,反应的化学方程式为2NH4Cl+Ca(OH)2 ![]() 2NH3+CaCl2+2H2O;一水合氨为弱碱,在水溶液中存在部分电离,电离出氢氧根离子使溶液显碱性,方程式为:NH3H2O
2NH3+CaCl2+2H2O;一水合氨为弱碱,在水溶液中存在部分电离,电离出氢氧根离子使溶液显碱性,方程式为:NH3H2O![]() NH4++OH-,向氨水中加入少量NH4Cl固体,c(NH4+)增大,平衡左移,即c(OH-)减小,pH值降低,加入少量明矾,明矾电离出的铝离子结合氢氧根生成氢氧化铝,促进氨水的电离,c(NH4+)增大,故答案为:2NH4Cl+Ca(OH)2
NH4++OH-,向氨水中加入少量NH4Cl固体,c(NH4+)增大,平衡左移,即c(OH-)减小,pH值降低,加入少量明矾,明矾电离出的铝离子结合氢氧根生成氢氧化铝,促进氨水的电离,c(NH4+)增大,故答案为:2NH4Cl+Ca(OH)2 ![]() 2NH3+CaCl2+2H2O;NH3H2O
2NH3+CaCl2+2H2O;NH3H2O![]() NH4++OH-;降低;增大;
NH4++OH-;降低;增大;
(2)硝酸铵分解生成N2O和H2O,达到平衡,说明为可逆反应,化学反应方程式为:NH4NO3![]() N2O+2H2O,250℃时,水为气体状态,故平衡常数K=c(N2O)×c2(H2O),NH4NO3中NH4+的N元素化合价为-3价,NO3-中的N元素的化合价为+5价,反应后N元素的化合价为+1价,发生归中反应,N元素由-3价升高到+1价,升高了4,因此反应中每分解1mol硝酸铵,转移电子数为4mol,故答案为:NH4NO3
N2O+2H2O,250℃时,水为气体状态,故平衡常数K=c(N2O)×c2(H2O),NH4NO3中NH4+的N元素化合价为-3价,NO3-中的N元素的化合价为+5价,反应后N元素的化合价为+1价,发生归中反应,N元素由-3价升高到+1价,升高了4,因此反应中每分解1mol硝酸铵,转移电子数为4mol,故答案为:NH4NO3![]() N2O+2H2O;K=c(N2O)×c2(H2O);4;
N2O+2H2O;K=c(N2O)×c2(H2O);4;
(3)pH=12的氨水的浓度大于0.01mol/L,pH=2的盐酸的浓度等于0.01mol/L,等体积混合后氨水过量,溶液呈碱性,故答案为:碱;
(4)由图可知,此反应反应物总能量高于生成物,且△H=209-348=-139kJmol-1,故答案为:-139。

 优等生题库系列答案
优等生题库系列答案