题目内容
【题目】三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点:33℃,沸点:73℃。实验室可用如图装置制取ICl3。
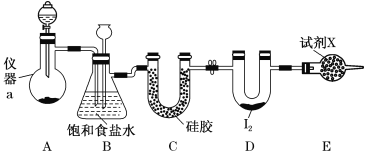
(1)仪器a的名称是________。
(2)制备氯气选用的药品为漂白精固体[主要成分为Ca(ClO)2]和浓盐酸,相关反应的化学方程式为__________________________________。
(3)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C中是否发生堵塞,请写出发生堵塞时装置B中的现象:____________________________________________。
(4)试剂X为________________。
(5)氯气与单质碘需在温度稍低于70℃下反应,则装置D适宜的加热方式为________________。
(6)500 mL(标准状况)含有CO的某气体样品通过盛有足量I2O5的干燥管,170℃下充分反应,用水-乙醇混合液充分溶解产物I2,定容到100 mL。取25.00 mL用0.0100 mol·L-1 Na2S2O3标准溶液滴定,消耗标准溶液20.00 mL,则样品中CO的体积分数为________。(保留三位有效数字)(已知:气体样品中其他成分与I2O5不反应;2Na2S2O3+I2===2NaI+Na2S4O6)
【答案】 蒸馏烧瓶 Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O 吸滤瓶中液面下降,长颈漏斗中液面上升 碱石灰 水浴加热 8.96%
【解析】实验室可用如图装置制取ICl3:装置A是Ca(ClO)2)和浓盐酸反应制取氯气,盐酸易挥发,反应制取的氯气中含有氯化氢、水蒸气等杂质,通过装置B中长导管内液面上升或下降调节装置内压强,B为安全瓶,可以防止倒吸,根据B中内外液面高低变化,可以判断是否发生堵塞,同时利用饱和食盐水除去氯气中的氯化氢,装置C是利用硅胶吸收水蒸气,装置D碘和氯气反应生成ICl3,氯气有毒需进行尾气处理,E装置吸收多余的氯气,防止污染空气.
(1)根据装置图可知仪器a的名称;
(2)次氯酸钙具有强的氧化性,能够氧化盐酸,生成氯化钙、氯气和水,依据化合价升级数目相同配平方程式;
(3)装置B作安全瓶,监测实验进行时C中是否发生堵塞,C发生堵塞时,B中压强增大,吸滤瓶中液面下降,长颈漏斗中液面上升;
(4)氯气有毒需进行尾气处理,可以用碱石灰吸收;
(5)水浴的温度不超过100℃,水浴能简便控制加热的温度,且能使受热容器受热均匀;
(6) 根据方程式:5CO+I2O5![]() 5CO2+I2和2Na2S2O3+I2=2NaI+Na2S4O6列关系式得:5CO~I2~2Na2S2O3;然后计算即可。
5CO2+I2和2Na2S2O3+I2=2NaI+Na2S4O6列关系式得:5CO~I2~2Na2S2O3;然后计算即可。
(1)根据装置图可知仪器a的名称为蒸馏烧瓶,
故答案为:蒸馏烧瓶;
(2)漂白粉固体和浓盐酸反应生成氯化钙、氯气和水,化学方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O;
故答案为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O;
(3)装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,发生堵塞时B中的压强增大,吸滤瓶中液面下降,长颈漏斗中液面上升,
故答案为:吸滤瓶中液面下降,长颈漏斗中液面上升;
(4)反应后剩余的氯气能够污染空气,不能排放到空气中,装置E为球形干燥管,装有固体药品碱石灰,吸收多余的氯气,防止污染空气,所以试剂X为碱石灰,
故答案为:碱石灰;
(5)因水浴能简便控制加热的温度,且能使受热反应试管受热均匀,由于氯气与单质碘需在温度稍低于70℃下反应,应采取水浴加热,
故答案为:水浴加热.
(6)由信息可知5CO+I2O5![]() 5CO2+I2,所以5CO~I2~2Na2S2O3即5CO~2Na2S2O3,n(CO)=
5CO2+I2,所以5CO~I2~2Na2S2O3即5CO~2Na2S2O3,n(CO)=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() ×4×(0.010 0 mol·L-1×0.02 L)=2×10-3mol,V(CO)=2×10-3mol×22.4 L·mol-1×1 000 mL·L-1=44.8 mL。
×4×(0.010 0 mol·L-1×0.02 L)=2×10-3mol,V(CO)=2×10-3mol×22.4 L·mol-1×1 000 mL·L-1=44.8 mL。
故样品中CO的体积分数=![]() ×100%=8.96%。
×100%=8.96%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案




