题目内容
【题目】已知电导率越大导电能力越强。常温下用0.100 mol·L-1NaOH溶液分别滴定10.00mL浓度均为0.100 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是
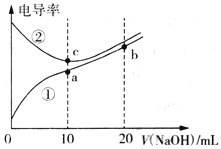
A. 曲线①代表滴定盐酸的曲线
B. a点溶液中: c(OH-)+c(CH3COO-)-c(H+) =0.1 mol/L
C. a、b、c三点溶液中水的电离程度:c>a>b
D. b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
【答案】D
【解析】醋酸为弱酸,等浓度时离子浓度比盐酸小,则导电性较弱,由此可知①为醋酸的变化曲线,②为盐酸的变化曲线,加入氢氧化钠,醋酸溶液离子浓度逐渐增大,导电性逐渐增强,盐酸发生中和反应,离子浓度减小,由图象可知加入氢氧化钠10mL时完全反应,对于离子浓度大小比较可以利用物料守恒和电荷守恒考虑解决。
由分析可知,曲线①代表滴定CH3COOH溶液的曲线,曲线②代表滴定HCl溶液的曲线,A选项错误;a点氢氧化钠与CH3COOH溶液恰好反应生成CH3COONa,a点溶液中c(Na+)=0.05mol/L,电解质溶液中都存在电荷守恒,根据电荷守恒得c(CH3COO-)+c(OH-)-c(H+)=c(Na+)=0.05mol/L,B选项错误;酸或碱抑制水的电离,含有弱酸根离子的盐促进水的电离,c点溶质为NaCl,a点溶质为醋酸钠,醋酸根离子促进水的电离,b点为等物质的量浓度的醋酸钠和NaOH的混合物,NaOH会抑制水的电离,所以在相同温度下,水的电离程度大小关系: b<c<a,C选项错误;b点为等物质的量浓度的醋酸钠和NaOH的混合物,根据电荷守恒:c(CH3COO-)+c(OH-)=c(H+)+c(Na+)和物料守恒:2c(CH3COO-)+2c(CH3COOH)= c(Na+)得:c(OH-)= c(H+)+c(CH3COO-)+2c(CH3COOH),所以有c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH),D选项正确;正确答案:D。

 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案