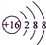
题目内容
2.某气态烃对氢气的相对密度为2,在氧气中完全燃烧1.16g这种烃,并将所得产物通过装有无水CaCl2的干燥管和装有碱石灰的干燥管,当称量这两个干燥管的质量时,它们依次增重1.8g和3.52g.该烃的分子式为( )| A. | CH4 | B. | C2H6 | C. | C3H8 | D. | C4H10 |
分析 根据相对密度计算该气态烃的相对分子质量,无水CaCl2的干燥管质量增重1.8g为生成水的质量,装有碱石灰的干燥管质量增3.52g为生成二氧化碳的质量,根据n=$\frac{m}{M}$计算该烃、二氧化碳、水的物质的量,根据原子守恒计算烃分子中C、H原子数目,然后确定其分子式.
解答 解:气态烃对空气(空气的平均相对分子质量为29)的相对密度为2,则该烃的相对分子质量为:29×2=58,
则该烃的物质的量=$\frac{1.16g}{58g/mol}$=0.02mol,
无水CaCl2的干燥管质量增重1.8g为生成水的质量,物质的量为$\frac{1.8g}{18g/mol}$=0.1mol,
装有碱石灰的干燥管质量增3.52g为生成二氧化碳的质量,物质的量为$\frac{3.52g}{44g/mol}$=0.08mol,
根据原子守恒可知烃分子中N(C)=$\frac{0.08mol}{0.02mol}$=4、N(H)=$\frac{0.1mol×2}{0.02mol}$=10,
故该烃的分子式为C4H10,
故选D.
点评 本题考查了有机物分子式确定的计算,题目难度中等,明确相对密度与相对分子质量的关系为解答关键,注意掌握质量守恒定律在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
12.把2.1g CO与H2组成的混合气体与足量的O2充分燃烧后,立即将产物全部通入到足量的Na2O2固体中,则固体的质量增加了( )
| A. | 2.1 g | B. | 3.6 g | C. | 7.2 g | D. | 无法确定 |
13.为了确定(NH4)2Fe(SO4)2•6H2O(硫酸亚铁铵晶体)的成分,下列实验操作及叙述中不正确的是( )
| A. | 取少量样品放入试管中,加热,试管口放一团蘸有无水硫酸铜粉末的棉花团,变蓝则可证明晶体的成分中含有结晶水 | |
| B. | 取少量样品溶于水,向溶液中滴入几滴新制氯水,再滴入2滴KSCN溶液,溶液变为红色,则可证明晶体的成分中含有Fe2+ | |
| C. | 取少量样品溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- | |
| D. | 取少量样品放入试管中,加入少量浓NaOH溶液并加热,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中是否含有NH4+ |
17.密闭容器中的可逆反应 H2(g)+I2(g)?2HI (g),能说明反应达到平衡的是( )
| A. | 容器内压强不变 | |
| B. | 单位时间内消耗1molH2,同时生成2molHI | |
| C. | 混合气体的颜色不变 | |
| D. | HI的浓度与I2的浓度相等 |
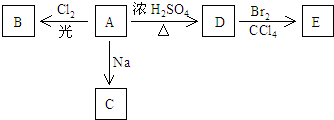
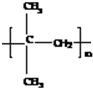 ;
; ;
; 向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定).
向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定). ,试写出:
,试写出: 短周期元素A、B、C、D、E、F、G原子序数依次递增,已知A和D,C和G为同一主族元素,D形成的阳离子和C形成的阴离子具有相同的核外电子排布,B原子的最外层电子数比次外层多3,G形成的化合物甲是造成酸雨的主要原因,F和A可形成化合物FA4很不稳定,F与C形成的化合物是制造光导纤维的主要原料,E的最高价氧化物的水化物能溶解于D的最高价氧化物的水化物中.请回答下列问题:
短周期元素A、B、C、D、E、F、G原子序数依次递增,已知A和D,C和G为同一主族元素,D形成的阳离子和C形成的阴离子具有相同的核外电子排布,B原子的最外层电子数比次外层多3,G形成的化合物甲是造成酸雨的主要原因,F和A可形成化合物FA4很不稳定,F与C形成的化合物是制造光导纤维的主要原料,E的最高价氧化物的水化物能溶解于D的最高价氧化物的水化物中.请回答下列问题: .画出G离子的结构示意图
.画出G离子的结构示意图