题目内容
12.电解普通水和重水(${\;}_{2}^{1}$H2O)的混合物,通电一段时间后,两极共生成气体18.5g,体积为33.6L(标况下).求所生成的气体中氕和氘的原子个数比是多少.分析 先根据氢气和氧气的体积之比为2:1,从而计算出氢气和氧气的体积以及各自物质的量,计算出氧气的质量,进而计算氢气总质量,再利用平均摩尔质量法计算普通氢和重氢的物质的量之比,结合分子构成计算重氢和普通氢的原子个数之比即可.
解答 解:电解水的方程式为2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑,由方程式知,氢气和氧气的体积之比为2:1,即氢气的体积为22.4L,氢气的物质的量为1mol;氧气的体积为11.2L,氧气的质量=$\frac{11.2L}{22.4L/mol}$×32g/mol=16g;氢气的质量为2.5g,所以氢气的平均摩尔质量=$\frac{2.5g}{1mol}$=2.5g/mol,普通氢和重氢的物质的量之比为: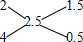 ,即为1.5:0.5=3:1,普通氢和重氢都是双原子分子,所以普通氢和重氢的原子个数之比为3:1;
,即为1.5:0.5=3:1,普通氢和重氢都是双原子分子,所以普通氢和重氢的原子个数之比为3:1;
答:生成的气体中氕和氘的原子个数比是3:1.
点评 本题以电解原理为载体,考查了化学方程式计算、物质的量的有关计算,难度不大,充分利用平均摩尔质量法是解答本题是关键,注意对十字相乘法的理解.

练习册系列答案
相关题目
2.在2L容积不变的容器中,发生N2+3H2?2NH3的反应.现通入4mol H2和4mol N2,10s内用H2表示的反应速率为0.12mol/(L•s),则10s后容器中N2的物质的量是( )
| A. | 1.6 mol | B. | 2.8 mol | C. | 3.2 mol | D. | 3.6 mol |
20.下列有关实验的叙述,正确的是( )
| A. | 分馏石油时,温度计的水银球必须插入液面下 | |
| B. | 用浓氨水洗涤做过银镜反应的试管 | |
| C. | 配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加直至沉淀刚好溶解为止 | |
| D. | 蔗糖水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖 |
7.钠、镁、铝三种金属单质的混合物跟足量的稀硫酸溶液充分反应后,得到标准状况下的氢气2.24L,则这三种金属的总物质的量可能是( )
| A. | 0.050 mol | B. | 0.060 mol | C. | 0.100 mol | D. | 0.200 mol |
17.下列有关元素周期表中的某些推断正确的是( )
| A. | 位于同一主族的元素的价电子数相同,则各元素的常见化合价也一定相同 | |
| B. | 碱金属族元素同卤族元素一样,其单质的熔沸点随元素原子序数的增大而逐渐升高 | |
| C. | 若x是ⅡB族中元素的原子序数,那么原子序数为x+1的元素是ⅢA族 | |
| D. | 在周期表中金属和非金属元素的分界线附近的元素是过渡元素 |
4.下列物质的电子式书写正确的是( )
| A. | 氯化氢  | B. | 二氧化碳  | ||
| C. | 氮气  | D. | 氯化镁  |
1.下列事实不能用勒夏特列原理解释的是( )
| A. | 增大压强能缩短碘化氢分解反应达到平衡的时间 | |
| B. | 配制硫酸铁溶液时,向溶液中加入少量硫酸 | |
| C. | 往醋酸溶液中加碱溶液,使c(CH3COO-) 增大 | |
| D. | 向水中加入酸可抑制水的电离 |
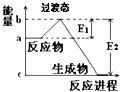 (1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是放热(填“吸热”或“放热”)反应,NO2和CO的总能量>(填“>”、“<”或“=”)CO2和NO的总能量.
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是放热(填“吸热”或“放热”)反应,NO2和CO的总能量>(填“>”、“<”或“=”)CO2和NO的总能量.