题目内容
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法正确的是( )
| X | Y | |
| Z | W |
| A、W单质与水反应,生成一种有漂白性物质 |
| B、最高价氧化物对应水化物酸性:Z>W>X |
| C、4种元素的氢化物中,Z氢化物最稳定 |
| D、原子半径:W>Z>Y>X |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由短周期元素X、Y、Z、W在元素周期表中的位置,可知X、Y处于第二周期,Z、W处于第三周期,Y原子的最外层电子数是次外层电子数的3倍,其最外层电子为6,则Y为O元素,可推知Z为N元素、Z为S元素、W为Cl元素,结合元素周期律与元素单质化合物性质解答.
解答:
解:由短周期元素X、Y、Z、W在元素周期表中的位置,可知X、Y处于第二周期,Z、W处于第三周期,Y原子的最外层电子数是次外层电子数的3倍,其最外层电子为6,则Y为O元素,可推知Z为N元素、Z为S元素、W为Cl元素,
A.氯气与水反应生成HCl与HClO,HClO具有漂白性,故A正确;
B.同周期自左而右元素非金属性增强,故非金属性Cl>S,非金属性越强,最高价含氧酸的酸性越强,故酸性HClO4>H2SO4,故B错误;
C.四种元素中Cl元素非金属性最强,故氢化物中HCl最稳定,故C错误;
D.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Z>W>X>Y,故D错误,
故选A.
A.氯气与水反应生成HCl与HClO,HClO具有漂白性,故A正确;
B.同周期自左而右元素非金属性增强,故非金属性Cl>S,非金属性越强,最高价含氧酸的酸性越强,故酸性HClO4>H2SO4,故B错误;
C.四种元素中Cl元素非金属性最强,故氢化物中HCl最稳定,故C错误;
D.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Z>W>X>Y,故D错误,
故选A.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素周期律的理解掌握,难度不大.

练习册系列答案
相关题目
丙烷和氯气发生取代反应生成二氯丙烷的同分异构体的数目有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
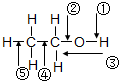 乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明不正确的是( )
乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明不正确的是( )| A、和金属钠反应时,键①断裂 |
| B、和浓硫酸共热至170℃时,键②和⑤断裂 |
| C、乙醇完全燃烧时,断裂键①② |
| D、在铜催化下和氧气反应时,键①和③断裂 |
下列说法不正确的说法是( )
| A、阿司匹林具有解热镇痛作用 |
| B、长期饮用纯净水,有可能引起一些微量元素缺乏症 |
| C、Al(OH)3能用于治疗胃酸过多 |
| D、使用青霉素时,直接静脉注射可以不用进行皮肤敏感测试 |
与反应Cl2+SO2+2H2O=H2SO4+2HCl中水的作用完全相同的是( )
A、2H2O
| ||||
| B、Cl2+H2O=HCl+HClO | ||||
C、3Fe+4H2O(g)
| ||||
| D、2Na+2H2O=2NaOH+H2↑ |
应用元素周期律的有关知识,可以预测我们不知道的一些元素及其化合物的性质.下列预测中不正确的是
( )
①Be的氧化物的水化物可能具有两性
②Tl能与盐酸和NaOH溶液作用,均产生氢气
③At单质为有色固体,At难溶于水易溶于四氯化碳
④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤SrSO4是难溶于水的白色固体
⑥H2Se是无色、有毒,比H2S稳定的气体.
( )
①Be的氧化物的水化物可能具有两性
②Tl能与盐酸和NaOH溶液作用,均产生氢气
③At单质为有色固体,At难溶于水易溶于四氯化碳
④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤SrSO4是难溶于水的白色固体
⑥H2Se是无色、有毒,比H2S稳定的气体.
| A、①②③④ | B、②④⑥ |
| C、①③⑤ | D、②④⑤ |
下列装置中(杯中均盛海水)铁腐蚀最快的是( )
A、 |
B、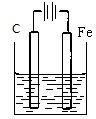 |
C、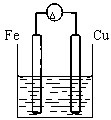 |
D、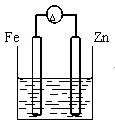 |
下列关于电解质溶液的叙述正确的是( )
| A、室温下,pH=3的氢氟酸加水稀释后,电离常数Ka(HF)和pH均减小 | ||
| B、室温下,将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) | ||
C、向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中
| ||
| D、室温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊试液呈红色 |