题目内容
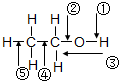 乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明不正确的是( )
乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明不正确的是( )| A、和金属钠反应时,键①断裂 |
| B、和浓硫酸共热至170℃时,键②和⑤断裂 |
| C、乙醇完全燃烧时,断裂键①② |
| D、在铜催化下和氧气反应时,键①和③断裂 |
考点:乙醇的化学性质
专题:有机物的化学性质及推断
分析:A、金属钠与乙醇反应取代羟基上氢原子;
B、乙醇和浓H2SO4共热至170℃时,碳氧键、与羟基所连的碳的相邻的碳上的碳氢键断裂;
C、燃烧时所有的化学键发生断裂.
D、乙醇在铜催化下和O2反应生成乙醛,结合结构式判断;
B、乙醇和浓H2SO4共热至170℃时,碳氧键、与羟基所连的碳的相邻的碳上的碳氢键断裂;
C、燃烧时所有的化学键发生断裂.
D、乙醇在铜催化下和O2反应生成乙醛,结合结构式判断;
解答:
解:A、金属钠与乙醇反应取代羟基上氢原子,反应时键①断裂,故A正确;
B、乙醇和浓H2SO4共热至170℃时,碳氧键、与羟基所连的碳的相邻的碳上的碳氢键断裂,反应时键②⑤断裂,故B正确;
C、燃烧时所有的化学键发生断裂,反应时①②③④⑤断裂,故C错误;
D、乙醇在铜催化下和O2反应生成乙醛,乙醇中的键①③断裂,故D正确;
故选C.
B、乙醇和浓H2SO4共热至170℃时,碳氧键、与羟基所连的碳的相邻的碳上的碳氢键断裂,反应时键②⑤断裂,故B正确;
C、燃烧时所有的化学键发生断裂,反应时①②③④⑤断裂,故C错误;
D、乙醇在铜催化下和O2反应生成乙醛,乙醇中的键①③断裂,故D正确;
故选C.
点评:本题考查有机物的结构与性质,侧重乙醇性质的考查,注意乙醇的性质与官能团、化学键的关系,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
当两个原子形成共价键时,原子的能量将( )
| A、都升高 |
| B、都降低 |
| C、都保持不变 |
| D、一个升高,一个降低 |
以NA表示阿伏伽德罗常数,下列说法中正确的是( )
| A、1mol 12C18O2中,所含的中子数为22NA |
| B、5.6g铁粉与酸反应失去的电子数一定为0.2NA |
| C、常温下,42g C2H4和C4H8的混合物中含有的碳原子数为3NA |
| D、标况下,11.2L SO3所含的分子数为0.5NA |
下列说法正确的是( )
| A、干冰和氨都属于弱电解质 |
| B、NO2和SO2都是形成酸雨的气体 |
| C、淀粉、纤维素和油脂都属于天然高分子化合物 |
| D、常温下,铁、铝遇到稀硝酸表面会生成一层致密的氧化膜,发生钝化 |
关于NaHCO3溶液,下列表述不正确的是( )
| A、c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| B、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| C、HCO3-的水解程度大于HCO3-的电离程度 |
| D、c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A、Na+、Cu2+、Cl-、NO3- |
| B、Na+、NO3-、H+、CO32- |
| C、MnO4-、K+、HCO3- |
| D、K+、Na+、Cl-、NO3- |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法正确的是( )
| X | Y | |
| Z | W |
| A、W单质与水反应,生成一种有漂白性物质 |
| B、最高价氧化物对应水化物酸性:Z>W>X |
| C、4种元素的氢化物中,Z氢化物最稳定 |
| D、原子半径:W>Z>Y>X |
锌-空气电池可能成为未来的理想动力源,该电池的电解质溶液可以是酸性或碱性.在碱性溶液中该电池总反应可表示为:2Zn+4NaOH+O2═2Na2ZnO2+2H2O.下列有关锌-空气电池说法正确的是( )
| A、碱性电解质溶液中正极反应式为:4OH--4e-═O2↑+2H2O |
| B、碱性或酸性电解质溶液中,该电池正极反应式相同 |
| C、该电池工作时,Na+移向负极 |
| D、每生成1mol ZnO22-转移电子数为2NA |
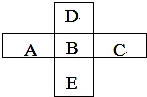 A、B、C、D、E五种主族元素所处周期表的位置如图所示.
A、B、C、D、E五种主族元素所处周期表的位置如图所示.