题目内容
3.X、Y都是芳香族化合物,均为常见食用香精,广泛用于化妆品、糖果及调味品中.1mol X水解得到1mol Y和1mol CH3CH2OH,X、Y的分子量都不超过200,完全燃烧都只生成CO2和H2O.且X分子中碳和氢元素总的质量百分含量约为81.8%,且碳与氢元素的质量比为11:1
(1)X、Y分子量之差为28.
(2)X的分子式是C11H12O2.
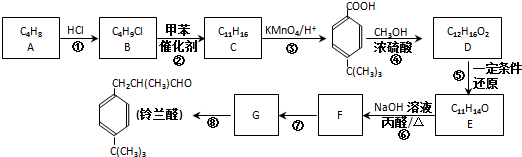
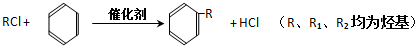
(3)G和X互为同分异构体,且具有相同的官能团,用芳香烃A合成G路线如下:
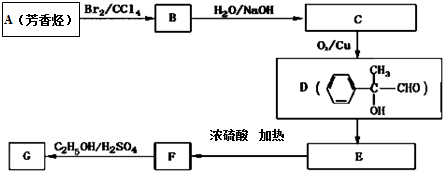
①写出A的结构简式
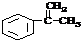 .
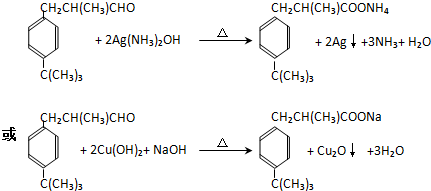
.②B→C的反应类型是取代反应,E→F反应的化学方程式为:
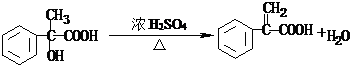 .
.③写出所有符合下列条件的F的同分异构体的结构简式:
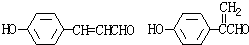 .
.ⅰ.分子内除了苯环无其他环状结构,且苯环上有2个对位取代基.
ⅱ.一定条件下,该物质既能与银氨溶液发生银镜反应又能和FeCl3溶液发生显色反应.
④某物质M与E同分异构体,写出M满足下列条件的同分异构体有20种
ⅰ、与FeCl3溶液发生显色反应
ⅱ、与碳酸氢钠溶液反应放出气体
ⅲ、苯环上有3条侧链.
分析 1molX水解得到1molY和1mol CH3CH2OH,X、Y的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O.且X分子中碳和氢元素总的质量百分含量约为81.8%,含O为$\frac{200×(1-81.8%×)}{16}$≈2,则X为酯,由D的结构可知,D→E发生催化氧化,E为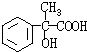 ,E→F发生消去反应,所以F为
,E→F发生消去反应,所以F为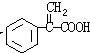 ,F与乙醇发生酯化反应生成G,则G为
,F与乙醇发生酯化反应生成G,则G为 ,G和X互为同分异构体,且具有相同的官能团,则X为
,G和X互为同分异构体,且具有相同的官能团,则X为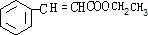 ,Y为
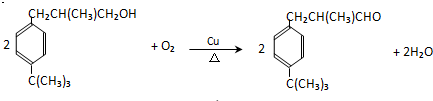
,Y为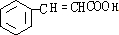 ,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为
,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为 ,然后结合有机物的结构和性质来解答.
,然后结合有机物的结构和性质来解答.
解答 解:1molX水解得到1molY和1mol CH3CH2OH,X、Y的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O.且X分子中碳和氢元素总的质量百分含量约为81.8%,含O为$\frac{200×(1-81.8%×)}{16}$≈2,则X为酯,由D的结构可知,D→E发生催化氧化,E为 ,E→F发生消去反应,所以F为
,E→F发生消去反应,所以F为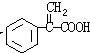 ,F与乙醇发生酯化反应生成G,则G为
,F与乙醇发生酯化反应生成G,则G为 ,G和X互为同分异构体,且具有相同的官能团,则X为
,G和X互为同分异构体,且具有相同的官能团,则X为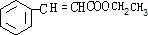 ,Y为
,Y为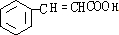 ,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为
,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为 ,
,
(1)X为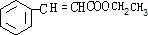 ,Y为
,Y为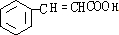 ,相差C2H4,即相对分子质量相差28,
,相差C2H4,即相对分子质量相差28,
故答案为:28;
(2)X为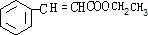 ,X的分子式为C11H12O2,
,X的分子式为C11H12O2,
故答案为:C11H12O2;
(3)①由上述分析可知A为 ,
,
故答案为: ;
;
②B→C的反应为卤代烃的碱性水解,是取代反应,E→F的反应为 ,
,
故答案为:取代反应; ;
;
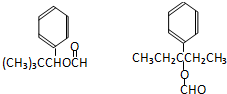
③F为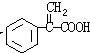 ,符合i.分子内除了苯环无其他环状结构,且苯环上有2个对位取代基,ii.一定条件下该物质既能与银氨溶液发生银镜反应又能和FeCl3溶液发生显色反应,其一取代基为-OH,则同分异构体为
,符合i.分子内除了苯环无其他环状结构,且苯环上有2个对位取代基,ii.一定条件下该物质既能与银氨溶液发生银镜反应又能和FeCl3溶液发生显色反应,其一取代基为-OH,则同分异构体为 ,
,
故答案为:
④E为 ,M与E同分异构体,M满足下列条件ⅰ、与FeCl3溶液发生显色反应,说明有酚羟基,ⅱ、与碳酸氢钠溶液反应放出气体,说明有羧基,ⅲ、苯环上有3条侧链,则M的结构为苯环上连有-OH、-COOH、-CH2CH3,或-OH、-CH2COOH、-CH3,根据定二动一的原则可知,每种情况都有10种结构,所以共有20种,
,M与E同分异构体,M满足下列条件ⅰ、与FeCl3溶液发生显色反应,说明有酚羟基,ⅱ、与碳酸氢钠溶液反应放出气体,说明有羧基,ⅲ、苯环上有3条侧链,则M的结构为苯环上连有-OH、-COOH、-CH2CH3,或-OH、-CH2COOH、-CH3,根据定二动一的原则可知,每种情况都有10种结构,所以共有20种,
故答案为:20.
点评 本题考查有机物的合成,注意有机物的官能团与性质的关系,结构与性质的关系、熟悉常见反应的反应原理即可解答,同分异构体为解答的难点,题目难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | KMnO4溶液用盐酸酸化并加入H2O2:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O | |
| B. | Fe2(SO4)3和Ba(OH)2溶液混合:Fe3++SO42-+Ba2++3OH-=BaSO4↓+Fe(OH)3↓ | |
| C. | 等体积等物质的量浓度的AlCl3、Ba(OH)2、HCl溶液混合:3H++Al3++6OH-=Al(OH)3↓+3H2O | |
| D. | 水玻璃与稀醋酸混合:SiO32-+2H+=H2SiO3↓ |
| A. | 氯气通入等物质的量溴化亚铁溶液中:2Cl2+2Fe2++2 Br-=4 Cl-+2Fe3++Br2 | |
| B. | 向苯酚溶液中滴加Na2CO3溶液: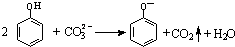 | |
| C. | 足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O=2HCO3- | |
| D. | 氨水吸收过量的SO2:SO2+2NH3•H2O=SO32-+2NH4++H2O |
| A. | Na与水反应 Na+2H2O=Na++2OH-+H2↑ | |
| B. | 向AlCl3溶液中加入过量的NaOH溶液 Al3++3OH-=Al(OH)3↓ | |
| C. | 氯气与烧碱溶液反应:Cl2+2OH-=Cl-+ClO-+H2O | |
| D. | 氢氧化钡溶液与硫酸溶液反应 Ba2++OH-+H++SO42-=BaSO4↓+H2O |
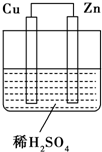 如图所示是Zn和Cu形成的原电池,其实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
如图所示是Zn和Cu形成的原电池,其实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )试验后的记录:
①Cu为负极,Zn为正极
②Cu极上有气泡产生
③SO42-向Cu移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu→Zn
⑥正极反应式:Cu-2e-=Cu2+.
| A. | ①②③ | B. | ②④ | C. | ④⑤⑥ | D. | ③④⑤ |
| A. | 可溶性铁盐、铝盐均可用于水的净化 | |
| B. | “开发利用新能源”、“汽车尾气催化净化”都能提高空气质量 | |
| C. | 电解NaCl溶液可制得金属钠 | |
| D. | 在海轮外壳上镶嵌上锌块,可减缓船体的腐蚀速率 |

 .
. .
. .
. .
. CO和H2作为重要的燃料和化工原料,有着十分广泛的应用.
CO和H2作为重要的燃料和化工原料,有着十分广泛的应用.