题目内容
18.下列反应的离子方程式正确的是( )| A. | 氯气通入等物质的量溴化亚铁溶液中:2Cl2+2Fe2++2 Br-=4 Cl-+2Fe3++Br2 | |
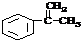
| B. | 向苯酚溶液中滴加Na2CO3溶液: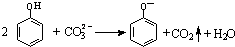 | |
| C. | 足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O=2HCO3- | |
| D. | 氨水吸收过量的SO2:SO2+2NH3•H2O=SO32-+2NH4++H2O |
分析 A.二价铁离子的还原性强于溴离子,氯气先氧化二价铁离子;
B.不符合反应的客观事实,苯酚与碳酸钠溶液反应生成碳酸氢钠;
C.足量的CO2通入饱和碳酸钠溶液中,生成碳酸氢钠沉淀;
D.二氧化硫过量反应生成亚硫酸氢铵.
解答 解:A.氯气通入等物质的量溴化亚铁溶液中,离子方程式:2Cl2+2Fe2++2 Br-=4 Cl-+2Fe3++Br2,故A正确;
B.向苯酚溶液中滴加Na2CO3溶液反应生成苯酚钠和碳酸氢钠,离子方程式:C6H5-OH+CO32-=C6H5-O-+HCO3-,故B错误;
C.足量的CO2通入饱和碳酸钠溶液中,反应生成碳酸氢钠沉淀,离子方程式:2Na++CO32-+H2O+CO2=2NaHCO3↓,故C错误;
D.氨水吸收过量的SO2,离子方程式:SO2+NH3•H2O=HSO3-+NH4+,故D错误;
故选:A.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子反应必须符合客观事实,题目难度不大.

练习册系列答案
相关题目
18.在稀硫酸中加入铜粉,铜粉不溶,再加入下列物质①FeCl3,②Fe2O3,③Cu(NO3)2,④KNO3,
铜粉溶解的是( )
铜粉溶解的是( )
| A. | 只有①或② | B. | 只有②或④ | C. | 只有①或②或③ | D. | 上述物质均可 |
9.下列叙述正确的是( )
| A. | 氢氧化铝、碳酸钠都是常见的胃酸中和剂 | |
| B. | 长期摄入肉、蛋、鱼偏多易导致血液偏酸性 | |
| C. | 碘酒中的碘因有还原性而起到杀菌消毒作用 | |
| D. | 碘盐、铁强化酱油等营养强化剂适合所有人食用 |
6.下列叙述正确的是( )
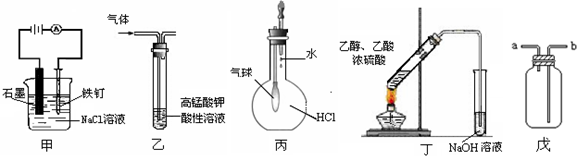
①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体.

①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体.
| A. | ①⑤ | B. | ②④ | C. | ③④ | D. | ③⑤ |
13.25℃时,H2SO3?HSO${\;}_{3}^{-}$+H+的电离平衡常数Kh=1×10-2,下列说法不正确的是( )
| A. | 该温度下NaHSO3 的水解平衡常数Kh=1×10-2 | |
| B. | 若向NaHSO3 溶液中加入少量的I2,则溶液中$\frac{c{(H}_{2}{SO}_{3})}{c(HS{O}_{3}^{-})}$ 将减小 | |
| C. | 略微升高温度 Ka(H2SO3)和 Kh(NaHSO3)均增大 | |
| D. | NaHSO3溶液中:c(H+)<c(S${O}_{3}^{2-}$)+c(HSO${\;}_{3}^{-}$)+c(OH-) |
7.下列物质中,只含有离子键的是( )
| A. | NaOH | B. | NH4Cl | C. | MgCl2 | D. | H2O |
8.碳及其化合物有广泛应用.
(1)工业冶炼铝,以石墨为阳极.阳极反应式为2O2--4e-=O2↑,可能发生副反应有C+O2$\frac{\underline{\;高温\;}}{\;}$CO2(或2C+O2$\frac{\underline{\;高温\;}}{\;}$2CO).
(2)一氧化碳和空气在酸性介质中构成燃料电池,负极反应式为.如果理论输出电压为1.50V,能量密度E=.
(3)向75mL 4mol•L-1KOH溶液中缓慢通入4480mL CO2气体(标准状况)恰好完全被吸收.①写出该反应的离子方程式:2CO2+3OH-=CO32-+HCO3-+H2O.
②该吸收溶液中离子浓度大小排序为c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
③常温下,a mol•L-1KHCO3溶液的pH=8,HCO3-的水解常数约等于$\frac{10{\;}^{-12}}{a-10{\;}^{-6}}$.(用含a式表示).
(4)已知:①2H2(g)+O2(g)=2H2O(l)△H1=-571.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
③CO(g)+2H2(g)═CH3OH(g)△H3=-90.8kJ•mol-1
计算甲醇蒸气的燃烧热△H=-763.8kJ•mol-1.
(5)某温度下,发生可逆反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.0kJ•mol-1
①向某容器中充入1.0molH2和1.0mol(g),在一定条件下发生上述反应.混合气体中CO的物质的量与时间关系如下列所示:
相对实验I,实验II可能改变的条件可能是,该温度下,平衡常数=1.
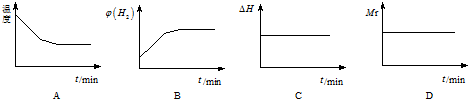
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应.
下列图象正确且说明可逆反应达到平衡状态的是A.(填序号)
(1)工业冶炼铝,以石墨为阳极.阳极反应式为2O2--4e-=O2↑,可能发生副反应有C+O2$\frac{\underline{\;高温\;}}{\;}$CO2(或2C+O2$\frac{\underline{\;高温\;}}{\;}$2CO).
(2)一氧化碳和空气在酸性介质中构成燃料电池,负极反应式为.如果理论输出电压为1.50V,能量密度E=.
(3)向75mL 4mol•L-1KOH溶液中缓慢通入4480mL CO2气体(标准状况)恰好完全被吸收.①写出该反应的离子方程式:2CO2+3OH-=CO32-+HCO3-+H2O.
②该吸收溶液中离子浓度大小排序为c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
③常温下,a mol•L-1KHCO3溶液的pH=8,HCO3-的水解常数约等于$\frac{10{\;}^{-12}}{a-10{\;}^{-6}}$.(用含a式表示).
(4)已知:①2H2(g)+O2(g)=2H2O(l)△H1=-571.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
③CO(g)+2H2(g)═CH3OH(g)△H3=-90.8kJ•mol-1
计算甲醇蒸气的燃烧热△H=-763.8kJ•mol-1.
(5)某温度下,发生可逆反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.0kJ•mol-1
①向某容器中充入1.0molH2和1.0mol(g),在一定条件下发生上述反应.混合气体中CO的物质的量与时间关系如下列所示:
| 0 | 5min | 10min | 15min | 20min | 25min | |
| I(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
| Ⅱ(800℃) | 1.0 | 0.7 | 0.60 | 0.50 | 0.50 | 0.50 |
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应.
下列图象正确且说明可逆反应达到平衡状态的是A.(填序号)

 .
. .
. .
.