题目内容
3.海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图: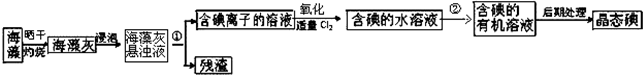
(1)指出制取碘的过程中有关的实验操作名称:①过滤;②萃取分液.写出通入适量Cl2后,有关反应的离子方程式Cl2+2I-═I2+2Cl-
(2)提取碘的过程中.可供选择的有机试剂是BC.
A.酒精 B.四氯化碳 C.苯 D.水
(3)为使海藻灰中碘离子转化为碘的有机溶液.实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器,尚缺少的玻璃仪器是普通漏斗、分液漏斗、锥形瓶.
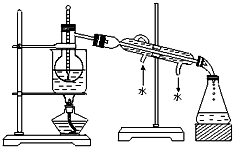
(4)从含碘的有机溶液中提取碘和回收有机溶液,还需经过蒸馏.观察上述实验装置,指出其中错误之处缺石棉网、温度计的水银球插入液面以下、冷凝管进出水方向颠倒.
(5)进行蒸馏操作时.使用水浴的原因是受热比较均匀,温度容易控制.最后晶态碘在蒸馏烧瓶里聚集.
分析 (1)分离固体和液体用过滤,利用溶解性的差异来分析,氯气氧化性强于碘,能把碘离子从其盐溶液中置换出来;
(2)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,萃取剂与溶质不反应,据此来选择合适的试剂;
(3)海藻灰中碘离子转化为碘的有机溶液,需要用到分液;
(4)冷凝水应是下进上出,烧杯加热应垫石棉网,温度计水银球应与烧瓶支管口相平;
(5)水浴加热的温度是使试管内或烧杯内试剂受热温度均匀,具有长时间加热温度保持恒定的特点.
解答 解:(1)过滤适用于不溶于水的固体和液体,分离固体和液体用过滤;将碘水中的碘单质萃取出来,选择合适的萃取剂即可,氯气氧化性强于碘,能把碘离子从其盐溶液中置换出来,离子反应方程式为:Cl2+2I-═I2+2Cl-,故答案为:过滤;萃取、分液;Cl2+2I-═I2+2Cl-;
(2)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,萃取剂与溶质不反应,碘在四氯化碳或苯中的溶解度大于在水中的溶解度,四氯化碳或苯和水都不互溶,且四氯化碳或苯和碘都不反应,故可用四氯化碳或苯,故答案为:BC;
(3)海藻灰中碘离子转化为碘的有机溶液,需要先溶解海藻灰,过滤得到含有碘离子的溶液,过滤需要普通漏斗,然后利用有机溶液萃取碘,需要用到分液,分液需要用到分液漏斗、锥形瓶,故答案为:普通漏斗、分液漏斗、锥形瓶;
(4)冷凝水应是下进上出,烧杯加热应垫石棉网,温度计水银球应与烧瓶支管口相平,
故答案为:缺石棉网、温度计的水银球插入液面以下、冷凝管进出水方向颠倒;
(5)水浴加热的温度是使试管内或烧杯内试剂受热温度均匀,具有长时间加热温度保持恒定的特点,四氯化碳沸点:76.8℃,碘单质沸点为184℃,所以最后晶态碘在蒸馏烧瓶里聚集,故答案为:受热比较均匀,温度容易控制; 蒸馏烧瓶.
点评 本题一海带中碘的制取为载体,主要考查了物质的分离和提纯,掌握过滤、萃取、蒸馏等操作是解答本题的关键,题目难度不大.

| A. | Cl2 | B. | SO2 | C. | H2S | D. | CO2 |
| A. | 两种原子,如果核外电子排布相同,则一定属于同种元素 | |
| B. | 两种微粒,若质量数不同,则其化学性质一定不同 | |
| C. | 两种微粒,若质量数相同,则其化学性质一定相同 | |
| D. | 微粒的核外电子数相同,则一定属于同种元素 |
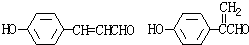
 膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )
膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )| A. | 芥子醇的分子式是C11H14O4,属于芳香烃 | |
| B. | 芥子醇分子中所有碳原子不可能在同一平面上 | |
| C. | 芥子醇不能使酸性KMnO4溶液褪色 | |
| D. | 芥子醇可以发生氧化反应、取代反应、加成反应 |
铜粉溶解的是( )
| A. | 只有①或② | B. | 只有②或④ | C. | 只有①或②或③ | D. | 上述物质均可 |
| A. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| B. | Fe与稀硫酸反应制取H2时,改用浓硫酸 | |
| C. | Al在氧气中燃烧生成A12O3,将Al片改成Al粉 | |
| D. | Na与水反应时增大水的用量 |
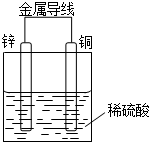 某同学设计出如下原电池原理和实验装置来证明Cu和Zn的金属活动性顺序.请你完成下列实验报告
某同学设计出如下原电池原理和实验装置来证明Cu和Zn的金属活动性顺序.请你完成下列实验报告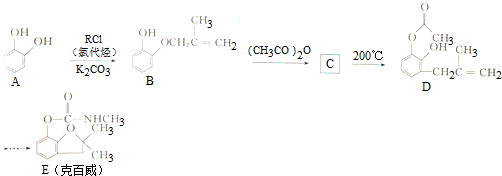
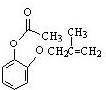 .
.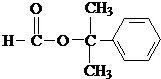 .
.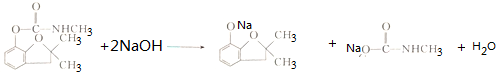 .
. 的两步化学方程式
的两步化学方程式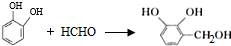 、
、 .
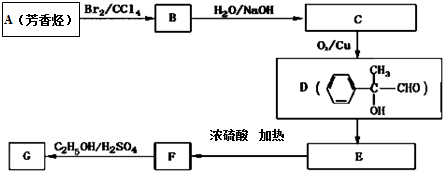
.
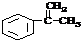 .
.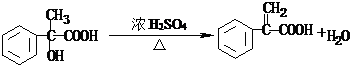 .
. .
.