题目内容
氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是( )
| A、1mol/L氢氰酸溶液能电离出H+ |
| B、HCN易溶于水 |
| C、10mL 1mol/L HCN恰好与10mL 1mol/L NaOH溶液完全反应 |
| D、在相同条件下,HCN溶液的导电性比强酸溶液的弱 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:氢氰酸为弱电解质,则利用其电离不完全来分析,一般测定溶液的pH或测定相同条件下与强酸的导电性比较以及对应盐溶液的酸碱性来判断.
解答:
解;A.能电离出H+,只能说明溶液呈酸性,不能证明酸性强弱,故A错误;
B.不能利用物质的溶解性来判断是否为弱电解质,即溶解性与电解质的强弱无关,故B错误;
C.二者物质的量相等,不能证明酸性的强弱,故C错误;
D.相同条件下,氢氰酸溶液的导电性比强酸溶液的弱,能说明氢氰酸电离不完全,为弱电解质,故D正确.
故选D.
B.不能利用物质的溶解性来判断是否为弱电解质,即溶解性与电解质的强弱无关,故B错误;
C.二者物质的量相等,不能证明酸性的强弱,故C错误;
D.相同条件下,氢氰酸溶液的导电性比强酸溶液的弱,能说明氢氰酸电离不完全,为弱电解质,故D正确.
故选D.
点评:本题考查弱电解质的判断方法,明确弱电解质在水中电离不完全是解答本题的关键,学生应注意在平时的学习中归纳判断弱电解质的方法,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列溶液中一定呈中性的是( )
| A、PH=7的溶液 |
| B、c(H+)=c( OH-)的溶液 |
| C、盐溶液 |
| D、既含有H+ 又含有OH-的溶液 |
“神舟六号”用动力燃料之一为氢化锂三兄弟--LiH、LiD、LiT.其中Li的质量数为7,有关下列叙述中正确的是( )
| A、三种物质质子数之比为1:2:3 |
| B、三种物质中子数之比为0:1:2 |
| C、三种物质的摩尔质量之比为4:5:6 |
| D、三种物质核外电子数之比为1:1:1 |
设NA代表阿伏加德罗常数,以下说法不正确的是( )
| A、18g水中含有电子数为10NA |
| B、16g氧气所含原子数为NA |
| C、4.8g金属镁变成镁离子时失去电子数为0.2NA |
| D、46g二氧化氮和46g四氧化二氮含有的原子数均是3NA |
标准状况下,2mol Cl2和2mol H2O相比较,下列叙述中正确的是( )
| A、分子数相等 | B、原子数相等 |
| C、体积相等 | D、质量相等 |
正确的实验设计和操作是实验成功的重要因素,下列实验设计或操作正确的是( )
A、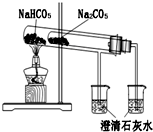 证明热稳定性Na2CO3>NaHCO3 |
B、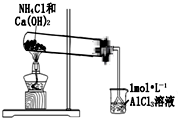 证明氢氧化铝的两性 |
C、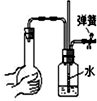 检查装置气密性 |
D、 测定KClO3元素的质量 |
下列离子反应方程式正确的是( )
| A、AlCl3溶液滴入到足量的氨水中:A13++4NH3?H2O═A1O2-+4NH4++2H2O |
| B、碳酸氢钙溶液中加入少量苛性钾溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| C、钠与水反应:Na+H2O═Na++OH-+H2↑ |
| D、过量二氧化碳通入氢氧化钠溶液中 CO2+OH-═HCO3- |
下列离子方程式中正确的是( )
| A、Fe(OH)3滴加稀盐酸:OH-+H+=H2O |
| B、向石灰乳[Ca(OH)2]溶液通入过量的二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O |
| C、MgCl2溶液中滴加氨水:Mg2++2OH-=Mg(OH)2↓ |
| D、NaHSO4溶液中加BaCl2溶液:SO42-+Ba2+=BaSO4↓ |