题目内容
标准状况下,2mol Cl2和2mol H2O相比较,下列叙述中正确的是( )
| A、分子数相等 | B、原子数相等 |
| C、体积相等 | D、质量相等 |
考点:阿伏加德罗常数,物质分子中的原子个数计算
专题:阿伏加德罗常数和阿伏加德罗定律
分析:根据N=nNA可知,等物质的量的氯气和水一定具有相同的分子数;由于二者分子中含有的原子数不同,所以含有的原子数目不同;二者摩尔质量不同,则含有的质量一定不相等;标准状况下水为液体,氯气为气体,二者的摩尔体积不同,所以具有的体积不相等.
解答:
解:A.2mol氯气和2mol水分子中都含有2NA个分子,含有的分子数相等,故A正确;
B.2mol氯气中含有4mol氯原子,2mol水中含有6mol原子,二者含有的原子数目不同,故B错误;
C.标准状况下,水不是气体,水的摩尔体积小于22.4L/mol,2mol水的体积小于44.8L,2mol氯气在标况下体积为22.4L,二者体积不相等,故C错误;
D.2mol氯气的质量为71g,2mol水的质量为36g二者的质量不相等,故D错误;
故选A.
B.2mol氯气中含有4mol氯原子,2mol水中含有6mol原子,二者含有的原子数目不同,故B错误;
C.标准状况下,水不是气体,水的摩尔体积小于22.4L/mol,2mol水的体积小于44.8L,2mol氯气在标况下体积为22.4L,二者体积不相等,故C错误;
D.2mol氯气的质量为71g,2mol水的质量为36g二者的质量不相等,故D错误;
故选A.
点评:本题考查有关物质的量的计算,题目难度不大,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
“化学是人类进步的关键”.下列有关说法能反映正确化学观点的是( )
| A、改变物质的性质不一定要通过化学变化 |
| B、天然物质都比人造物质好 |
| C、一种元素可有多种离子,但只有一种原子 |
| D、根据分散系是否具有丁达尔效应,分散系分为溶液、胶体和浊液 |
下列离子方程式正确的是( )
| A、实验室中制取CO2:CO32-+2H+═CO2↑+H2O |
| B、钠投入CuSO4溶液中:2Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑ |
| C、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
| D、向酸性KMnO4溶液中滴加双氧水:2MnO4-+H2O2+6H+═2Mn2++3O2↑+4H2O |
氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是( )
| A、1mol/L氢氰酸溶液能电离出H+ |
| B、HCN易溶于水 |
| C、10mL 1mol/L HCN恰好与10mL 1mol/L NaOH溶液完全反应 |
| D、在相同条件下,HCN溶液的导电性比强酸溶液的弱 |
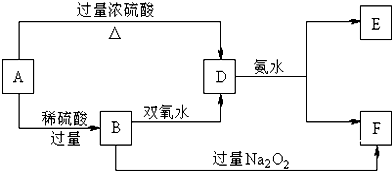
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )


| A、X可能是一种氢化物 |
| B、M不可能是金属 |
| C、E可能是一种有色气体 |
| D、X→Y一定是非氧化还原反应 |
下列说法不正确的是( )
| A、利用分液漏斗进行分液操作时,先打开分液漏斗旋塞,使下层液体慢慢流出,待下层液体完全流出后,关闭旋塞,上层液体再从上面倒出 |
| B、固体药品取用:块状固体用镊子夹取,粉末状的用药匙或纸槽转移 |
| C、在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、环形玻璃搅拌棒进行搅拌、酸和过量的碱充分反应、取2-3次的实验平均值,以达到良好的实验效果 |
| D、用标准浓度的盐酸滴定未知浓度NaOH溶液时,酸式滴定管未用同浓度盐酸润洗,将导致测定结果偏低 |
下列反应的离子方程式正确的是( )
| A、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ |
| B、氧化铝溶于氢氧化钠:Al2O3+2OH-═2AlO2-+H2↑ |
| C、硅酸钠溶液中滴加稀盐酸:SiO32-+2H+═H2SiO3↓ |
| D、将氨水滴入到FeCl3溶液中:Fe3++3OH-═Fe(OH)3↓ |
某单质能与足量的浓HNO3反应放出NO2气体,若参加反应的单质和硝酸的物质的量之比为1:a,则该元素在反应中所显示的化合价是( )
| A、+2a | ||
| B、+a | ||
C、+
| ||
D、+
|