题目内容
6.Mg,Mg2+两种粒子中不相同的是( )①核内质子数
②核外电子数
③最外层电子数
④核外电子层数.
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
分析 Mg有12个质子,12个电子,3个电子层,最外层2个电子;
Mg2+有12个质子,10个电子,2个电子层,最外层8个电子,据此解答.
解答 解:Mg有12个质子,12个电子,3个电子层,最外层2个电子;
Mg2+有12个质子,10个电子,2个电子层,最外层8个电子,
二者具有相同的质子数,核外电子数、最外层电子数、电子层数都不相同,
故选:D.
点评 本题考查了镁原子与镁离子的区别,熟悉二者原子的构成是解题关键,题目难度不大.

练习册系列答案
相关题目
19.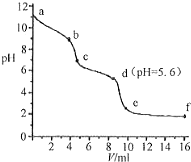 常温下,将已知浓度的盐酸滴定到未知浓度的Na2CO3溶液,用pH传感器测得混合溶液的pH变化曲线,如图所示:(已知饱和CO2溶液的pH为5.6)下列说法正确的是( )
常温下,将已知浓度的盐酸滴定到未知浓度的Na2CO3溶液,用pH传感器测得混合溶液的pH变化曲线,如图所示:(已知饱和CO2溶液的pH为5.6)下列说法正确的是( )
 常温下,将已知浓度的盐酸滴定到未知浓度的Na2CO3溶液,用pH传感器测得混合溶液的pH变化曲线,如图所示:(已知饱和CO2溶液的pH为5.6)下列说法正确的是( )
常温下,将已知浓度的盐酸滴定到未知浓度的Na2CO3溶液,用pH传感器测得混合溶液的pH变化曲线,如图所示:(已知饱和CO2溶液的pH为5.6)下列说法正确的是( )| A. | a点时,溶液呈碱性的原因是CO32-发生水解反应,其离子方程式为:CO32-+2H2O=H2CO3+2OH- | |
| B. | a→b段,溶液有气体放出 | |
| C. | c点以后,盐酸过量 | |
| D. | d点溶液中c(Na+)=c(Cl-) |
14.关于反应:
①2C2H2(g)+5O2(g)=4CO2 (g)+2H2O(l)△H=-2600kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1
③CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+216kJ•mol-1下列叙述正确的是( )
①2C2H2(g)+5O2(g)=4CO2 (g)+2H2O(l)△H=-2600kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1
③CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+216kJ•mol-1下列叙述正确的是( )
| A. | 2C2H2(g)+3O2(g)=4CO (g)+2H2O(l)△H=+1468 kJ•mol-1 | |
| B. | 在③反应时,若加入催化剂,可以使△H减小 | |
| C. | 若有3.2g CH4与足量水蒸汽按③反应,则放出热量是43.2 kJ | |
| D. | 若生成相同质量的CO2,则放出的热量C2H2大于CO |
1. 将1.00mol•L-1 NaOH溶液滴入20.00mL 1.00mol•L-1的一元酸HA溶液中,测得混合溶液的pH和温度随加入NaOH溶液体积变化曲线如图所示.下列说法正确的是( )
将1.00mol•L-1 NaOH溶液滴入20.00mL 1.00mol•L-1的一元酸HA溶液中,测得混合溶液的pH和温度随加入NaOH溶液体积变化曲线如图所示.下列说法正确的是( )
 将1.00mol•L-1 NaOH溶液滴入20.00mL 1.00mol•L-1的一元酸HA溶液中,测得混合溶液的pH和温度随加入NaOH溶液体积变化曲线如图所示.下列说法正确的是( )
将1.00mol•L-1 NaOH溶液滴入20.00mL 1.00mol•L-1的一元酸HA溶液中,测得混合溶液的pH和温度随加入NaOH溶液体积变化曲线如图所示.下列说法正确的是( )| A. | 室温时,HA的电离度约为10-6 | |
| B. | 图中B点时,溶液的KW略大于1×10-14 | |
| C. | 图中C点时,溶液中c(A-)=c(Na+)>c(H+)=c(OH-) | |
| D. | 图中D点后,溶液温度略下降的主要原因是生成的 NaA水解吸热 |
11.下列关于有机化合物的说法正确的是( )
| A. | 戊烷有两种同分异构体 | |
| B. | 乙烷,乙醇和苯均不能使酸性高锰酸钾褪色 | |
| C. | 乙醇,乙酸和乙酸乙酯可用碳酸钠溶液加以区别 | |
| D. | 乙烯,聚氯乙烯和苯分子均含有碳碳双键 |
18.除去试管中银镜的实验方案如下表所列,实验操作中均经振荡、充分反应:
下列分析结论正确的是( )
| 方案 | 实验操作 | 现象 |
| Ⅰ | 将2mL 2mol/L Fe(NO3)3溶液加入有银镜的试管中 | 银镜较迅速消失 试管口产生红棕色气体 |
| Ⅱ | 将2mL2mol/L Fe2(SO4)3溶液加入有银镜的试管中 | 银镜减少但未消失 |
| Ⅲ | 将2mL 2mol/L FeCl3溶液加入有银镜的试管中 | 银镜较迅速消失 有白色沉淀生成 |
| A. | 方案Ⅰ说明Fe3+ 氧化了Ag | |
| B. | 方案Ⅱ涉及反应之一为Fe3++Ag?Fe2++Ag+ | |
| C. | 方案Ⅱ、Ⅲ对比说明SO42-比Cl-更易沉淀Ag+ | |
| D. | 三个方案对比说明方案Ⅰ是除去银镜的最佳方案 |
15.已知NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1mol铁与铝的混合物与足量稀硫酸反应时,转移电子数是3NA | |
| B. | 18g重水(D2O)含有的电子数为9NA | |
| C. | pH=2的醋酸加水稀释到10倍后,溶液中H+数目大于0.001NA | |
| D. | 标准状况下,NA个CH3OH分子的体积约是22.4L |
13.甲烷和乙烯的混合气体100mL,能催化加氢气30mL,则混合气体中含有甲烷( )
| A. | 50mL | B. | 70mL | C. | 30mL | D. | 15mL |
