题目内容
【题目】下列反应的离子方程式正确的是( )
A.氨气通入醋酸溶液中CH3COOH+NH3= CH3COONH4
B.氢氧化钠与氯化铵溶液混合加热:![]() +OH-= NH3·H2O
+OH-= NH3·H2O
C.氨水中加盐酸:NH3·H2O+H+=![]() +H2O
+H2O
D.硫酸铵与氢氧化钡溶液:![]() +OH-= NH3·H2O
+OH-= NH3·H2O
【答案】C
【解析】
A. 氨气通入醋酸溶液中生成醋酸铵,铵盐易溶于水,应该拆成铵根离子和醋酸根离子,离子反应为:CH3COOH+NH3= CH3COO-+NH4+,故A错误;
B.氢氧化钠与氯化铵溶液混合加热会有氨气逸出,必须写成氨气形式,离子反应为:![]() +OH-= NH3↑+H2O,故B错误;
+OH-= NH3↑+H2O,故B错误;
C. 氨水中加盐酸生成氯化铵和水,离子反应为:NH3·H2O+H+=![]() +H2O,故C正确;
+H2O,故C正确;
D.硫酸铵与氢氧化钡溶液反应生成氨气、水和硫酸钡,硫酸钡不溶于水,不能拆成离子,生成物中要有硫酸钡出现,离子反应为:2![]() +SO42-+2OH-+Ba2+=2NH3·H2O+ BaSO4↓, D错误;
+SO42-+2OH-+Ba2+=2NH3·H2O+ BaSO4↓, D错误;
答案选C。

【题目】某兴趣小组制备一定量的乙酸乙酯.取3mL无水乙醇,2mL浓硫酸,2mL冰醋酸进行实验,用5mL饱和碳酸钠溶液收集产物。
I.实验装置如图所示
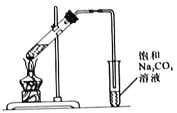
(1)制备乙酸乙酯的化学方程式为_______________。
(2)浓硫酸的作用是_______________。
(3)长导管的作用是_______________。
(4)接收装置还可选择下图中的___________。(填序号).
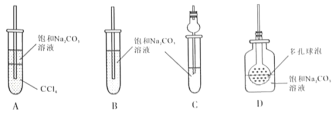
Ⅱ.甲同学用含有酚酞的饱和碳酸钠溶液(呈碱性)收集产物后振荡,发现红色迅速退去.
甲同学认为是蒸出的乙酸中和了碳酸钠.乙同学通过查阅资料并进行如下实验,证明甲同学的推测是错误的。
已知:酚酞难溶于水,易溶于有机溶剂;酚酞试剂是酚酞的乙醇溶液.
实验i,取振荡后的下层无色液体,分成两份,分别完成以下实验
序号 | 实验操作 | 实验现象 | 结论 |
1 | 滴加几滴酸酞试剂 | 溶液 ① (填“变红”成“不变红”) | 碳酸钠并未被乙酸完全中和,仍有大量剩余 |
2 | 滴入乙酸溶液 | 有大量气泡产生 |
实验ii.取振荡后的上层液体,加入 ② 溶液,振荡,发现出现浅红色,静置分层后红色消失。
实验iii,取5mL饱和碳酸钠溶液,滴入几滴酚酞试剂,再加入3mL乙酸乙酯(不含乙酸)振荡,溶液先变红,振荡后红色消失。回答下列问题
(5)完成上述实验:①_______________。②_______________。
(6)结合实验ii和实验iii的现象,可得出的结论是_______________。
(7)实验iii的实验目的是_______________。