题目内容
【题目】某兴趣小组制备一定量的乙酸乙酯.取3mL无水乙醇,2mL浓硫酸,2mL冰醋酸进行实验,用5mL饱和碳酸钠溶液收集产物。
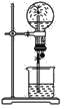
I.实验装置如图所示
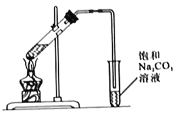
(1)制备乙酸乙酯的化学方程式为_______________。
(2)浓硫酸的作用是_______________。
(3)长导管的作用是_______________。
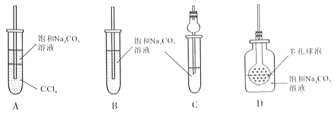
(4)接收装置还可选择下图中的___________。(填序号).
Ⅱ.甲同学用含有酚酞的饱和碳酸钠溶液(呈碱性)收集产物后振荡,发现红色迅速退去.
甲同学认为是蒸出的乙酸中和了碳酸钠.乙同学通过查阅资料并进行如下实验,证明甲同学的推测是错误的。
已知:酚酞难溶于水,易溶于有机溶剂;酚酞试剂是酚酞的乙醇溶液.
实验i,取振荡后的下层无色液体,分成两份,分别完成以下实验
序号 | 实验操作 | 实验现象 | 结论 |
1 | 滴加几滴酸酞试剂 | 溶液 ① (填“变红”成“不变红”) | 碳酸钠并未被乙酸完全中和,仍有大量剩余 |
2 | 滴入乙酸溶液 | 有大量气泡产生 |
实验ii.取振荡后的上层液体,加入 ② 溶液,振荡,发现出现浅红色,静置分层后红色消失。
实验iii,取5mL饱和碳酸钠溶液,滴入几滴酚酞试剂,再加入3mL乙酸乙酯(不含乙酸)振荡,溶液先变红,振荡后红色消失。回答下列问题
(5)完成上述实验:①_______________。②_______________。
(6)结合实验ii和实验iii的现象,可得出的结论是_______________。
(7)实验iii的实验目的是_______________。
【答案】CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O 催化剂、吸水剂 导气、冷凝 CD 变红 碳酸钠溶液 酚酞被萃取到乙酸乙酯层中 作对照实验,验证酚酞褪色的原因不是因为乙酸与碳酸钠反应
CH3COOC2H5+H2O 催化剂、吸水剂 导气、冷凝 CD 变红 碳酸钠溶液 酚酞被萃取到乙酸乙酯层中 作对照实验,验证酚酞褪色的原因不是因为乙酸与碳酸钠反应
【解析】
I.(1)实验室用乙酸和乙醇反应制取乙酸乙酯,依据酯化反应的反应历程是羧酸脱羟基、醇脱氢书写;
(2)根据乙酸与乙醇在加热、浓硫酸作催化剂的条件下发生酯化反应生成乙酸乙酯,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(3)长导管的作用是导气、冷凝乙酸乙酯;
(4)乙酸乙酯中常混有乙醇和乙酸,乙醇易溶于水、乙酸能与较快与碳酸钠反应,所以接收装置应该有防倒吸作用;
II.(5)甲同学认为是蒸出的乙酸中和了碳酸钠,乙同学通过实验证明下层无色液体是否含有碳酸钠或上层液体中是否含有酚酞,若下层无色液体含有碳酸钠或上层液体中含有酚酞,则证明甲同学的推测错误;
(6)通过实验ⅲ的对照实验,说明实验ii中上层液体中的酚酞被乙酸乙酯萃取;
(7)根据实验ⅱ和实验ⅲ的现象可知,酚酞褪色的原因是酚酞进入乙酸乙酯层中,不是因为碳酸钠消耗完全。
I.(1)乙酸与乙醇在浓硫酸作用下加热发生反应生成乙酸乙酯和水,反应的化学方程式为:CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案为:CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(2)乙酸与乙醇在加热、浓硫酸作催化剂的条件下发生酯化反应生成乙酸乙酯,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,则浓硫酸的作用为催化剂、吸水剂;
故答案为:催化剂、吸水剂;
(3)长导管的作用是导气、充分冷凝乙酸乙酯,
故答案为:导气、冷凝;
(4)乙酸乙酯中常混有乙醇和乙酸,需要除去,但乙醇易溶于水、乙酸能与较快与碳酸钠反应,所以可能出现倒吸现象,
A. 生成的乙酸乙酯和随之挥发过来的乙酸和乙醇都是有机物,通入CCl4中会发生倒吸,而且CCl4能溶解乙酸乙酯,使产率降低,故A不符合题意;
B. 直接通入饱和碳酸钠溶液中,可能出现倒吸,故B不符合题意;
C. 干燥管体积较大,可防倒吸,同时插入液面下,除杂更充分、彻底,故C符合题意;
D. 图中多孔球泡能防倒吸,同时可增大与碳酸钠溶液的接触面积,除杂效果更好,故D符合题意;
故答案为:CD;
II.(5)乙同学通过实验证明下层无色液体是否含有碳酸钠,碳酸钠溶液呈碱性,可加入酚酞,根据结论碳酸钠并未被乙酸完全中和,仍有大量剩余可知,酚酞变红;根据酚酞难溶于水,易溶于有机溶剂的信息,证明上层液体中是否含有酚酞,溶液变成浅红色,静置分层后红色消失,则加入的是碳酸钠等碱性物质,
故答案为:变红;碳酸钠溶液;
(6)通过实验ⅲ的对照实验,说明实验ii中上层液体含有酚酞,即实验ii中上层液体中的酚酞被乙酸乙酯萃取,
故答案为:酚酞被萃取到乙酸乙酯层中;
(7)根据实验ⅱ和实验ⅲ的现象可知,酚酞褪色的原因是酚酞进入乙酸乙酯层中,不是因为乙酸与碳酸钠反应,所以该实验的目的为作对照实验,验证酚酞褪色的原因不是因为乙酸与碳酸钠反应,而是酚酞进入乙酸乙酯层中,
故答案为:作对照实验,验证酚酞褪色的原因不是因为乙酸与碳酸钠反应。

【题目】氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点;氢气也是重要的化工原料。
(1)纳米级的Cu2O可作为太阳光分解水的催化剂。一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气发生反应:2H2O(g)![]() 2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同时段产生O2的量见表格:
2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同时段产生O2的量见表格:
时间/min | 20 | 40 | 60 | 80 |
n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
上述反应过程中能量转化形式为光能转化为____能,达平衡过程中至少需要吸收光能___kJ(保留三位小数)。
(2)氢气是合成氨工业的原料,合成塔中每产生2 molNH3,放出92.2kJ热量。已知:

则1 molN—H键断裂吸收的能量约等于_____。