题目内容
11.现有短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和为5.X元素原子最外层上的电子数是Y元素原子最外层与Z元素原子最外层电子数之和;Y元素最外层上电子数是其电子层数的2倍,X和Z可以形成XZ3型化合物,请回答问题:(1)X的名称氮、,Y的名称碳,Z的名称氢.
(2)XZ3的化学式为NH3,电子式为
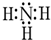 ,分子间存在氢键.
,分子间存在氢键.(3)X最高价氧化物对应水化物的浓溶液与红热的Y单质反应的化学方程式为4HNO3(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O.
分析 短周期中的三种元素X、Y、Z,原子序数依次减小,原子核外电子层数之和是5,则Z处于第一周期,X、Y处于第二周期,可推知Z为H元素;Y元素原子的最外层电子数是它的电子层数的2倍,则其最外层电子数为4,则Y为C元素,其最高正价等于最低负价;X元素原子的最外层电子数是Y和Z两元素原子的最外层电子数的总和,X最外层电子数为4+1=5,则X为氮元素,能与H元素形成NH3,据此答题;
解答 解:短周期中的三种元素X、Y、Z,原子序数依次减小,原子核外电子层数之和是5,则Z处于第一周期,X、Y处于第二周期,可推知Z为H元素;Y元素原子的最外层电子数是它的电子层数的2倍,则其最外层电子数为4,则Y为C元素,其最高正价等于最低负价;X元素原子的最外层电子数是Y和Z两元素原子的最外层电子数的总和,X最外层电子数为4+1=5,则X为氮元素,能与H元素形成NH3,
(1)由上述分析可知,X、Y、Z三种元素的元素名称分别为:氮、碳、氢,
故答案为:氮;碳;氢;
(2)XZ3的化学式为NH3,NH3的电子式是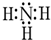 ,NH3分子之间存在氢键,
,NH3分子之间存在氢键,
故答案为:NH3;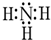 ;氢;
;氢;
(3)X最高价氧化物对应水化物的浓溶液为浓硝酸,与红热的碳单质反应的化学方程式为4HNO3(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O,
故答案为:4HNO3(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O.
点评 本题考查结构性质与位置关系,推断元素是解题的关键,注意根据最外层电子数之和确定Z是推断的突破口,难度不大.

练习册系列答案
相关题目
1.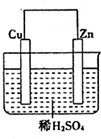 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:在卡片上,描述合理的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:在卡片上,描述合理的是( )
卡片:NO.28Date:2007.4.8
实验后的记录:
①Zn为阳极,Cu为阴极②H+向负极移动
③电子流动方向Zn→Cu④Cu极有H2产生
⑤若有1mol电子流过导线,则产生H2为0.5mol.
⑥正极的电极反应式:Zn-2e-═Zn2+.
 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:在卡片上,描述合理的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:在卡片上,描述合理的是( )卡片:NO.28Date:2007.4.8
实验后的记录:
①Zn为阳极,Cu为阴极②H+向负极移动
③电子流动方向Zn→Cu④Cu极有H2产生
⑤若有1mol电子流过导线,则产生H2为0.5mol.
⑥正极的电极反应式:Zn-2e-═Zn2+.
| A. | ①②③ | B. | ③④⑤ | C. | ④⑤⑥ | D. | ②③④ |
2.在2L容积不变的容器中,发生N2+3H2?2NH3的反应.现通入4mol H2和4mol N2,10s内用H2表示的反应速率为0.12mol/(L•s),则10s后容器中N2的物质的量是( )
| A. | 1.6 mol | B. | 2.8 mol | C. | 3.2 mol | D. | 3.6 mol |
6.下表为元素周期表的一部分,a、b、c…为部分元素.回答下列问题:
(1)请写出上述元素d3+的核外电子排布式1s222s2p63s23p63d5;
(2)请写出j的单质与a、h形成的化合物发生反应的化学方程式Cl2+H2O=HCl+HClO;
(3)请比较b、e、j三种元素的电负性由大到小的顺序Cl>Al>Mg(写元素符号);此三种元素的第一电离能由大到小的顺序Cl>Mg>Al(写元素符号);
(4)g、e两种元素的最高价氧化物对应的水合物的化学性质相似,请写出e元素最高价氧化物对应的水合物与a、c、h三种元素形成的化合物反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O;
(5)j、k、l三种元素之间能以原子个数比1:1两两形成互化物,这些互化物的性质类似于这些元素单质的性质.请写出k、l的互化物的电子式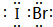 ,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).
,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).
| a | |||||||||||||||||
| f | h | i | |||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | k | ||||||||||||||
| l | |||||||||||||||||
(2)请写出j的单质与a、h形成的化合物发生反应的化学方程式Cl2+H2O=HCl+HClO;
(3)请比较b、e、j三种元素的电负性由大到小的顺序Cl>Al>Mg(写元素符号);此三种元素的第一电离能由大到小的顺序Cl>Mg>Al(写元素符号);
(4)g、e两种元素的最高价氧化物对应的水合物的化学性质相似,请写出e元素最高价氧化物对应的水合物与a、c、h三种元素形成的化合物反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O;
(5)j、k、l三种元素之间能以原子个数比1:1两两形成互化物,这些互化物的性质类似于这些元素单质的性质.请写出k、l的互化物的电子式
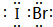 ,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).
,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).
20.下列有关实验的叙述,正确的是( )
| A. | 分馏石油时,温度计的水银球必须插入液面下 | |
| B. | 用浓氨水洗涤做过银镜反应的试管 | |
| C. | 配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加直至沉淀刚好溶解为止 | |
| D. | 蔗糖水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖 |
1.下列事实不能用勒夏特列原理解释的是( )
| A. | 增大压强能缩短碘化氢分解反应达到平衡的时间 | |
| B. | 配制硫酸铁溶液时,向溶液中加入少量硫酸 | |
| C. | 往醋酸溶液中加碱溶液,使c(CH3COO-) 增大 | |
| D. | 向水中加入酸可抑制水的电离 |