题目内容
11.细心的小红同学发现:I2的沸点竟然低于其熔点,这说明了碘单质(填物理性质)升华;从硫单质和食盐的混合物中采用升华方法获得纯净的碘单质.分析 碘的沸点比熔点低,易升华,可用升华的方法分离.
解答 解:I2的沸点竟然低于其熔点,这说明了碘单质易升华;从硫单质和食盐的混合物中采用升华的方法获得纯净的碘单质.
故答案为:升华;升华.
点评 本题考查混合物分离提纯方法的选择,为高频考点,把握混合物中物质的性质、性质差异为解答的关键,侧重混合物分离方法的考查,注意氯化铵的性质,题目难度不大.

练习册系列答案
相关题目
19.下列说法不正确的是( )
| A. | 等质量的N02与N204,所含质子数一定相等 | |
| B. | 等体积的N2O与NO2的原子总数一定相等 | |
| C. | 等物质的量的02与03的质量比为2:3 | |
| D. | 分子中含有相等原子数的NH3与H2的电子数之比为5:2 |
6.欲使NaCl、NH4Cl和SiO2的混合物分开,其必要的操作为( )
| A. | 升华、溶解、过滤、蒸发 | B. | 溶解、过滤、蒸发、分液 | ||
| C. | 加热、溶解、过滤、结晶 | D. | 溶解、过滤、分馏、结晶 |
16.在0.1mol/L的HA溶液中存在如下电离平衡:HA?A-+H+,对于该溶液,下列叙述正确的是( )
| A. | 滴加少量1.0mol/L HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减少 | |
| B. | 加水,溶液中c(H+)、c(A-)、c(HA)浓度均减小 | |
| C. | 加入少量NaA固体,平衡向逆反应方向移动,溶液中c(H+)增大 | |
| D. | 加入少量NaOH固体,平衡向正反应方向移动,溶液中c(H+)增大 |
3.下列说法正确的是( )
| A. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃的条件下△H应该不相同 | |
| B. | 化学反应中的能量变化都表现为热量变化 | |
| C. | 任何放热反应在常温下一定能发生 | |
| D. | 反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
20.下列说法正确的是( )
| A. | 7.8 g Na2O2中含有的阴离子数为0.1NA | |
| B. | 常温下,含0.1 mol碳酸钠的溶液中含有CO${\;}_{3}^{2-}$的个数为0.1NA | |
| C. | 7.8 g Na2S和Na2O2的混合物中,含有的阳离子数目为0.1NA | |
| D. | 12 g NaHSO4晶体中阳离子和阴离子的总数为0.3NA |
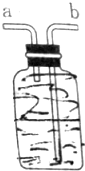 如图所示装置,用排空气法收集O2,O2应由b(填“a”或“b”下同)口进入,检验O2是否收集满的操作是将带火星的木条靠近a,如果带火星木条复燃,证明氧气收集满;若想用排水法收集O2,可将装置中充满水,O2由a口进入.
如图所示装置,用排空气法收集O2,O2应由b(填“a”或“b”下同)口进入,检验O2是否收集满的操作是将带火星的木条靠近a,如果带火星木条复燃,证明氧气收集满;若想用排水法收集O2,可将装置中充满水,O2由a口进入.