题目内容
【题目】某溶液X含有H+、Al3+、NH4+、Fe2+、Fe3+、HCO3-、S2-、SO42-、Cl-、OH-中的一种或几种,取该溶液进行实验,实验内容和相关数据(气体体积在标准状况下测定)如下:
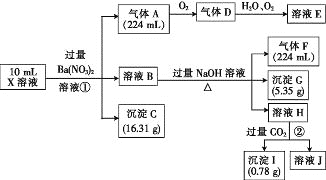
(1)通过上述实验过程,一定不存在的离子是_______。
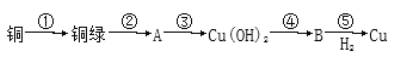
(2)反应①中生成A的离子方程式为________。
(3)若测得X溶液中c(H+)=6mol·L-1,则X溶液中_______(填“含”或“不含”)Fe3+,c(Fe3+)=________mol·L-1(若填不含,则不需计算),X溶液中c(Cl-)=_______mol·L-1。
【答案】HCO3-、S2-、OH- 3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O 含 2 8
【解析】
测得X溶液中c(H+)=6mol/L,在强酸性溶液中与H+反应的离子不能大量存在;一定不会存在HCO3-、S2-、OH-离子,加入过量硝酸钡生成沉淀,则沉淀C为BaSO4 沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E 为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量 NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于 CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,沉淀G为Fe(OH)3,说明原溶液中含有Al3+离子,通过计算氢氧化铁物质的量和原溶液中亚铁离子物质的量判断原溶液中含有Fe3+,溶液显酸性,溶液中含有Fe2+离子,就一定不含NO3-离子,根据已知溶液中电荷守恒计算确定是否含有的离子Cl-,以此解答。
通过上述分析可知:气体A是NO,溶液B中含有Al3+、NH4+、Fe2+,沉淀C是BaSO4,气体D是NO2,溶液E为HNO3,气体F是NH3,I为Al(OH)3,H为NaAlO2,沉淀G为Fe(OH)3:
(1)由于测得X溶液中c(H+)=6mol/L,溶液显酸性,在强酸性溶液中与H+反应的离子HCO3-、S2-、OH-不能大量存在;故原溶液一定不会存在HCO3-、S2-、OH-离子;
(2)在X中含有Fe2+、H+,当加入Ba(NO3)2溶液时,会发生氧化还原反应,产生Fe3+、NO、H2O,反应的离子方程式:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)n(NO)=0.224L÷22.4L/mol=0.01mol,根据3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O中Fe2+与NO的关系可知n(Fe2+)=3n(NO)=0.03mol,n[Fe(OH)3]=5.35g÷107g/mol=0.05mol>n(Fe2+)=0.03mol,根据Fe元素守恒,说明在原溶液中含有Fe3+,其物质的量是0.02mol,由于溶液的体积是0.01L,所以c(Fe3+)=0.02mol÷0.01L=2mol/L;该溶液中,n(H+)=6mol/L×0.01L=0.06mol,根据元素守恒可得n(NH4+)=n(NH3)=0.224L÷22.4L/mol=0.01mol,n(SO42-)=n(BaSO4)=16.31g÷233g/mol=0.07mol,n(Al3+)=n[Al(OH)3]=0.78g÷78g/mol=0.01mol,根据(3)计算可知n(Fe2+)=0.03mol,n(Fe3+)=0.02mol,由于正电荷总数:3n(Al3+)+ 3n(Fe3+)+2n(Fe2+)+ n(NH4+)+ n(H+)=3×0.01mol+3×0.02mol+2×0.03mol+0.01mol+0.06mol=0.22mol,n(SO42-)=0.07mol,其所带的负电荷数0.07mol×2=0.14mol<0.22mol,所以该溶液中还含有带负电荷的Cl-,其物质的量为n(Cl-)=0.22mol-0.14mol=0.08mol,其物质的量浓度c(Cl-)=0.08mol÷0.01L=8mol/L。

【题目】二苯基乙二酮常用作医药中间体及紫外线固化剂,可由二苯基羟乙酮氧化制得,相关物质的物理参数、化学方程式及装置图(加热和夹持装置已略去)如下:
相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/gcm-3 | 溶解性 | ||
二苯基羟乙酮 | 212 | 133 | 344 | 1.310 | 不溶于冷水,溶于乙醇 | |
二苯基乙二酮 | 210 | 97 | 348 | 1.084 | 不溶于水,能溶于乙醇 |
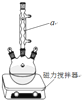
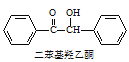 +2FeCl3
+2FeCl3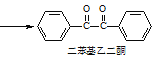 +2FeCl2+2HCl
+2FeCl2+2HCl
在反应装置中,加入10mL冰醋酸、5.50g FeCl3固体、10mL水及少量碎瓷片,加热至沸腾,停止加热,待沸腾平息后加入2.12g二苯基羟乙酮,继续加热回流至二苯基羟乙酮完全反应。反应结束后加水煮沸,冷却后即有二苯基乙二酮粗产品析出,用70%乙醇水溶液重结晶提纯,得到1.80g产品。
重结晶过程如下:
加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
请回答以下问题:
(1)装置图中仪器a的名称是____,其作用是____。
(2)加入碎瓷片的作用是____。若加热后发现未加碎瓷片,应采取的正确方法是___。
(3)实验中可采用薄层色谱跟踪反应进程,其原理和操作与纸上层析类同,通过观察薄层色谱展开后的斑点(在实验条件下,只有二苯基羟乙酮和二苯基乙二酮能够产生斑点)判断样品中的成分。如图分别为加入二苯基羟乙酮后反应开始、回流15min、30min、45min和60min时,用毛细管取样、点样,薄层色谱展开后的斑点:

该实验条件下加热____后可认为反应结束。
A.15min B.30min C.45min D.60min
(4)上述重结晶过程中,____(填步骤名称)操作除去了不溶性杂质。
(5)在重结晶过程中,不可选用明火直接加热,原因是____。
(6)不选择蒸馏的方法提纯二苯基乙二酮粗产品的原因是_____。
(7)本实验的产率是____%。(保留3位有效数字)
【题目】下列表述不正确的是
A | B | C | D |
|
|
|
|
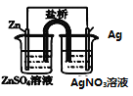
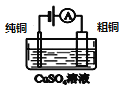
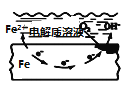
盐桥中的Cl-移向AgNO3溶液 | a极附近产生的气体能使湿润的淀粉碘化钾试纸变蓝 | 纯铜的电极反应式为:Cu2++2e-=Cu | 正极反应式为: O2+2H2O+4e-=4OH- |
A. AB. BC. CD. D