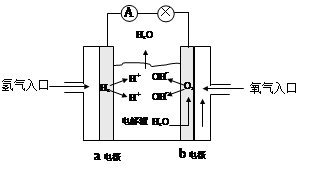
��Ŀ����
(14��)�����⻯�����MH��Ni�������������ܡ���ȫ������Ⱦ������ЧӦ���۸����ˣ��ѳ�ΪĿǰ��߷�չǰ���ġ���ɫ��Դ�����֮һ������ܷ�ӦΪMH+NiOOH  M+Ni(OH)2��MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ𡣵������ҺΪŨKOH��Һ��
M+Ni(OH)2��MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ𡣵������ҺΪŨKOH��Һ��
(1)д���ŵ�ʱ�ĸ�����Ӧ_________________
(2)���ʱ�������ĵ缫��ӦΪ__________________
����������������Ni(OH)2��̼�ۡ���������Ϳ�����������Ƴɡ�ij��ȤС��Ըõ�ص缫���Ͻ�����Դ�����о������ʵ���������£�
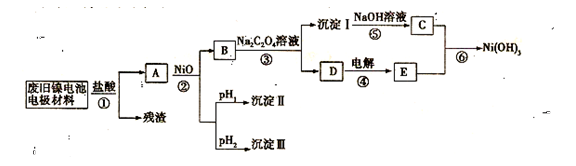
��֪����NiCl2������ˮ��Fe3+��������Ni2+
��ij�¶���һЩ�������������Ksp����������������pH���±���ʾ��
�ش��������⣺
��3�������ϱ������жϲ�����������ij�����Ϊ ���������ij���Ϊ��Ϊ__________________���ѧʽ������pH1 pH2�����>������=����<������
��4����֪�ܽ�ȣ�NiC2O4 > NiC2O4��H2O > NiC2O4��2H2O����۵Ļ�ѧ����ʽ�� ��
��5�����������ĵ缫��ӦΪ ����֤����������Լ�Ϊ ��
��6����д�������ӷ���ʽ ��
 M+Ni(OH)2��MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ𡣵������ҺΪŨKOH��Һ��
M+Ni(OH)2��MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ𡣵������ҺΪŨKOH��Һ��(1)д���ŵ�ʱ�ĸ�����Ӧ_________________
(2)���ʱ�������ĵ缫��ӦΪ__________________
����������������Ni(OH)2��̼�ۡ���������Ϳ�����������Ƴɡ�ij��ȤС��Ըõ�ص缫���Ͻ�����Դ�����о������ʵ���������£�

��֪����NiCl2������ˮ��Fe3+��������Ni2+
��ij�¶���һЩ�������������Ksp����������������pH���±���ʾ��
| M(OH)x | Ksp | pH | |
| ��ʼ���� | ������ȫ | ||
| Al(OH)3 | 1.9��10-23 | 3.43 | 4.19 |
| Fe(OH)3 | 3.8��10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6��10-14 | 7.60 | 9.75 |
�ش��������⣺
��3�������ϱ������жϲ�����������ij�����Ϊ ���������ij���Ϊ��Ϊ__________________���ѧʽ������pH1 pH2�����>������=����<������
��4����֪�ܽ�ȣ�NiC2O4 > NiC2O4��H2O > NiC2O4��2H2O����۵Ļ�ѧ����ʽ�� ��
��5�����������ĵ缫��ӦΪ ����֤����������Լ�Ϊ ��
��6����д�������ӷ���ʽ ��
(1) MH-e-+OH-=H2O+M (2)Ni(OH)2-e-+OH-=NiOOH+H2O (3)Fe(OH)3 Al(OH)3 ��
��4��NiCl2 + Na2C2O4 + 2H2O = NiC2O4. 2H2O�� + 2NaCl
��5��2Cl��2e-=Cl2�������۵⻯����Һ�������������𰸣���
��6��2Ni(OH)2 + 2OH- + Cl2 = 2Ni(OH)3+ 2Cl-
��4��NiCl2 + Na2C2O4 + 2H2O = NiC2O4. 2H2O�� + 2NaCl
��5��2Cl��2e-=Cl2�������۵⻯����Һ�������������𰸣���
��6��2Ni(OH)2 + 2OH- + Cl2 = 2Ni(OH)3+ 2Cl-
�����������1���ŵ�ʱ����������������Ӧ�����Ե缫��ӦΪ��MH-e-+OH-=H2O+M��
��2�����ʱ����������������Ӧ�����Ե缫��ӦΪ��Ni(OH)2-e-+OH-=NiOOH+H2O
��3������Ksp���Կ�����pH����ʱ��Fe(OH)3���ȳ�����Ȼ����Al(OH)3�����Ni(OH)2�����Բ�����������ij���II��Fe(OH)3�������ij���III��Al(OH)3��pH1< pH2��
��4�������ܽ�ȿ�֪NiC2O4��2H2O���ܽ����С�����Ԣ۵Ļ�ѧ����ʽΪNiCl2 + Na2C2O4 + 2H2O = NiC2O4. 2H2O�� + 2NaCl��
��5�����ݿ�ͼ��֪DΪNaCl��Һ�����Ե��ʱ������ӦΪ2Cl��2e-=Cl2�����������������õ��۵⻯����Һ��
��6�����ݿ�ͼ��֪CΪNi(OH)2�����Ԣ����ӷ���ʽΪ��2Ni(OH)2+2OH-+Cl2=2Ni(OH)3+
2Cl-��
�����������ۺ���ǿ���ѶȽϴ���Ҫ����ѧ���ķ��������ͽ����������Ǹ߿����ȵ�ϰ�⡣

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ

 3Zn(OH)2 + 2Fe(OH)3 + 4KOH��������������ȷ����
3Zn(OH)2 + 2Fe(OH)3 + 4KOH��������������ȷ���� 2CO32����6H2O��������˵����ȷ����
2CO32����6H2O��������˵����ȷ����