题目内容
一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:
2CH3OH + 3O2+4OH-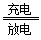 2CO32-+6H2O,则下列说法正确的是
2CO32-+6H2O,则下列说法正确的是
2CH3OH + 3O2+4OH-
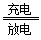 2CO32-+6H2O,则下列说法正确的是
2CO32-+6H2O,则下列说法正确的是| A.构成该电池的正极和负极必须是两种活性不同的金属 |
| B.充电时有CH3OH生成的电极为阴极 |
| C.放电时电解质溶液的pH逐渐增大 |
| D.放电时负极的电极反应为:CH3OH-6e-+8OH-= CO32-+6H2O |
BD
该电池是燃料电池,所以两电极不一定两种活性不同的金属,A不正确。充电相当于电解池,根据方程式可知,充电时,甲醇是CO32-的还原产物,因此甲醇在阴极生成,B正确。放电相当于原电池,根据方程式可知,放电时消耗OH-,所以pH减小,C不正确。原电池中负极失去电子,所以甲醇在负极通入,D正确。答案选BD。

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
 2PbSO4+2H2O。下列说法正确的是
2PbSO4+2H2O。下列说法正确的是 M+Ni(OH)2,M为储氢合金,MH为吸附了氢原子的储氢合金。电解质溶液为浓KOH溶液。
M+Ni(OH)2,M为储氢合金,MH为吸附了氢原子的储氢合金。电解质溶液为浓KOH溶液。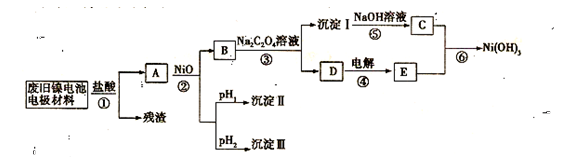

 Pb+PbO2+2H2SO4,下列判断不正确的是( )
Pb+PbO2+2H2SO4,下列判断不正确的是( )