籾朕坪否
‐籾朕/厮岑HCN(aq)嚥NaOH(aq)郡哘伏撹1 mol屎冦議ΔH﹆⇩12.1 kJ/mol◉膿磨、膿珠議蓮卑匣郡哘議嶄才犯ΔH﹆⇩57.3 kJ,mol⇩1。夸HCN壓邦卑匣嶄窮宣議ΔH吉噐↙ ⇄
A⤴⇩69.4 kJ,mol⇩1 B⤴⇩45.2 kJ,mol⇩1
C⤴⇦69.4 kJ,mol⇩1 D⤴⇦45.2 kJ,mol⇩1
‐基宛/D
‐盾裂/
編籾蛍裂⦿〙HCN(aq)⇦NaOH(aq)=NaCN(aq)⇦H2O(l) @H=⇩12.1kJ,mol⇩1,〖H⇦(aq)⇦OH⇩(aq)=H2O(l) @H=⇩57.3kJ,mol⇩1⇧〗HCN(aq)![]() H⇦(aq)⇦CN⇩(aq)⇧〙⇩〖誼竃〗⇧軸@H=(⇩12.1⇦57.3)kJ,mol⇩1=⇦45.2kJ,mol⇩1⇧絞僉𡸴D屎鳩。
H⇦(aq)⇦CN⇩(aq)⇧〙⇩〖誼竃〗⇧軸@H=(⇩12.1⇦57.3)kJ,mol⇩1=⇦45.2kJ,mol⇩1⇧絞僉𡸴D屎鳩。

膳楼過狼双基宛
屢購籾朕
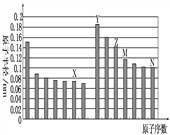
‐籾朕/和燕葎圷殆巓豚燕議匯何蛍,萩歌孚圷殆〙゛∇壓燕嶄議了崔,喘晒僥喘囂指基和双諒籾⦿
怛 巓豚 | IA | 0 | ||||||
1 | 〙 | ÅA | ‰A | ♯A | ♭A | ♪A | †A | |
2 | 〖 | 〗 | ∠ | |||||
3 | ⊥ | ⌒ | ∂ | ∇ | ||||
↙1⇄貧峰噴嶽圷殆嶄⇧恷互勺剳晒麗邦晒麗磨來恷膿議晒栽麗議晒僥塀頁___________⇧↙野晒僥憲催⇧和揖⇄⇧恷互勺剳晒麗邦晒麗珠來恷膿議晒栽麗議晒僥塀頁_____________⇧恷互勺剳晒麗邦晒麗𠮟曾來議狽剳晒麗議晒僥塀頁_____________。
↙2⇄〗嚥∠議賑蓑狽晒麗議糧協來喇寄欺弌議乏會頁_____________。
↙3⇄∠、⊥、⌒議宣徨磯抄喇寄欺弌議乏會頁__________________。
↙4⇄〙、〗侘撹議剩宣徨議窮徨塀頁______________。
↙5⇄〙、∠、⊥、∇嶄議蝶乂圷殆辛侘撹屡根宣徨囚嗽根自來慌勺囚議晒栽麗⇧亟竃凪嶄匯嶽晒栽麗議窮徨塀⦿______________。