题目内容
10.25°C和101kpa时,甲烷、乙烯和乙炔组成的混合烃30mL与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体的总体积缩小了55mL,原混合烃中乙炔的体积分数为( )| A. | 25% | B. | 33.3% | C. | 66.7% | D. | 75% |
分析 发生反应为:CH4+2O2=CO2+2H2O,C2H4+3O2=2CO2+2H2O,C2H2+$\frac{5}{2}$O2=2CO2+H2O,除去水蒸气,恢复到原来的温度和压强,根据反应方程式可知,CH4和C2H4反应后体积缩小的量是相同的,故可将两者看成是一种物质,设CH4和C2H4一共为xmL,C2H2为ymL,利用气体体积缩小了55mL及混合气体的体积来列等式计算出乙炔的体积,进而计算乙炔的体积分数.
解答 解:除去水蒸气,恢复到原来的温度和压强,则:
CH4+2O2=CO2+2H2O?△V
1 2 1 2
C2H4+3O2=2CO2+2H2O?△V
1 3 2 2
C2H2+$\frac{5}{2}$O2=2CO2+H2O△V
1 2.5 2 1.5
CH4和C2H4反应后体积缩小的量是相同的,故可将两者看成是一种物质,
设CH4和C2H4一共为xmL,C2H2为ymL,则:x+y=30、2x+1.5y=55,
联立解得:x=20、y=10,
则原混合烃中乙炔的体积分数为:$\frac{10mL}{30mL}$×100%≈33.3%,
故选B.
点评 本题考查混合物反应的计算,题目难度中等,解得关键是根据方程式判断体积变化,把甲烷与乙烯看作一个组分,从而转化为两组分混合,注意差量法的应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.在常温下,把一个盛有等物质的量的甲烷和氯气的密闭玻璃容器放在光亮的地方,两种气体充分反应,下列叙述中不正确的是( )
| A. | 容器内原子总数不变 | |
| B. | 足够长时间后容器内氯化氢分子数最少 | |
| C. | 容器内气体颜色变浅 | |
| D. | 容器内分子总数不变 |
18.有机物中碳原子和氢原子个数比为3:4,不能与溴水反应却能使KMnO4酸性溶液褪色.其蒸气密度是相同状况下甲烷密度的7.5倍.在溴化铁存在时与溴反应,能生成两种一溴代物.该有机物可能是( )
| A. | CH≡C-CH3 | B. | 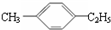 | C. | CH2=CHCH3 | D. | 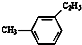 |
5.下列反应中,属于加成反应的是( )
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| B. | CH2=CH2+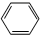 $\stackrel{一定条件}{→}$ $\stackrel{一定条件}{→}$ | |
| C. | CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH | |
| D. |  +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$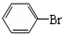 +HBr +HBr |
15.化学与生产、生活密切相关,下列叙述正确的是( )
| A. | 碘的升华、溴水中萃取溴、石油的分馏、煤的干馏均属于物理变化 | |
| B. | BaSO4难溶于水,属于弱电解质,在医学上用作钡餐 | |
| C. | “埃博拉”病毒在常温下较稳定,对热有中等度抵抗力,56℃不能完全灭活,60℃30min 方能破坏其感染性,此过程主要发生了蛋白质的变性 | |
| D. | 明矾和氯气均用于水的消毒、杀菌 |
2.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1NaAlO2溶液:Al3+、Na+、Cl-、NO3- | |
| B. | 加入金属铝产生H2的溶液中:NH4+、K+、SO42-、NO3- | |
| C. | 含有大量ClO-的溶液中:K+、Na+、NO3-、SO42- | |
| D. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO32- |
19.下列对相应有机物的描述完全正确的是( )
①甲烷:天然气的主要成分,能发生取代反应
②乙烯:一个国家石油化工发展水平的标志,可以发生加成反应
③苯:平面结构,每个分子中含有3个碳碳双键
④油脂:属于高分子化合物,可以发生水解反应
⑤淀粉:属于糖类物质,遇碘元素变蓝色
⑥蛋白质:遇浓硝酸显黄色,水解的最终产物为氨基酸.
①甲烷:天然气的主要成分,能发生取代反应
②乙烯:一个国家石油化工发展水平的标志,可以发生加成反应
③苯:平面结构,每个分子中含有3个碳碳双键
④油脂:属于高分子化合物,可以发生水解反应
⑤淀粉:属于糖类物质,遇碘元素变蓝色
⑥蛋白质:遇浓硝酸显黄色,水解的最终产物为氨基酸.
| A. | ①②③ | B. | ②④⑥ | C. | ①⑤⑥ | D. | ①②⑥ |
20.下列各组离子在指定溶液中能够大量共存的是( )
| A. | 无色溶液:K+、Al3+、NO3-、HCO3- | |
| B. | 常温下c(H+)/c(OH-)=1×10-12的溶液:Na+、K+、AlO2-、CO32- | |
| C. | 强酸性溶液:NH4+、Na+、SO32-、NO3- | |
| D. | 加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- |
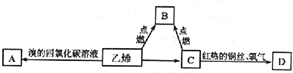
 ,乙烯燃烧时的现象是火焰明亮,伴有黑烟,放热;
,乙烯燃烧时的现象是火焰明亮,伴有黑烟,放热;