题目内容
12.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 含有0.1 mol•L-1Fe3+的溶液中:K+、Mg2+、I-、SO42- | |
| B. | c(Al3+)=0.5 mol•L-1的溶液中:Na+、K+、AlO2-、SO42- | |
| C. | 能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl- | |
| D. | 能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3- |
分析 离子之间能反应生成气体、沉淀、弱电解质或发生氧化还原反应、复分解反应的不能大量共存,据此分析解答.
解答 解:A.Fe3+和I-发生氧化还原反应而不能共存,故A错误;
B.Al3+、AlO2-发生双水解反应而不能大量共存,故B错误;
C.能使酚酞试液变红色说明溶液呈碱性,这几种离子之间不反应,且和氢氧根离子不反应,所以能大量共存,故C正确;
D.能溶解氢氧化铝的溶液呈酸性或碱性,酸性条件下,HCO3-不能大量共存,碱性条件下,铵根离子和HCO3-不能大量共存,故D错误;
故选C.
点评 本题考查离子共存,为高频考点,侧重考查复分解反应、氧化还原反应,明确离子共存条件及离子性质是解本题关键,易错选项是B.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.我国是一个淡水资源比较匮乏的国家,下列方法能直接从海水制取可饮用水的是( )
| A. | 萃取 | B. | 结晶 | C. | 蒸馏 | D. | 过滤 |
7.以NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA | |
| B. | 0.1mol Na2SO4溶液中,含有SO42-数为0.1NA | |
| C. | 46gNO2和N2O4混合气体中,含有氧原子总数为3NA | |
| D. | 0.5L 1mol/LNaCl溶液中含有的钠离子浓度1mol/L |
17.下表是元素周期表的一部分,请用元素符号或化学式回答有关问题:
(1)表中化学性质最不活泼的元素是Ar,最活泼的金属元素是K,最活泼的非金属元素是F.
(2)表中能形成两性氧化物的元素是Al,写出该元素的单质与⑨最高价氧化物的水化物反应的离子方程式2Al+2OH-+2H2O═2AlO2-+3H2↑.
(3)③⑥⑦三种元素原子半径由大到小的顺序是S>Cl>F.
(4)用电子式表示由元素⑨⑦形成化合物的过程:K++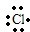 →
→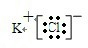 .
.
(5)③元素与⑩元素两者核电荷数之差是26.
(6)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表.
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)表中能形成两性氧化物的元素是Al,写出该元素的单质与⑨最高价氧化物的水化物反应的离子方程式2Al+2OH-+2H2O═2AlO2-+3H2↑.
(3)③⑥⑦三种元素原子半径由大到小的顺序是S>Cl>F.
(4)用电子式表示由元素⑨⑦形成化合物的过程:K++
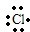 →
→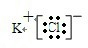 .
.(5)③元素与⑩元素两者核电荷数之差是26.
(6)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表.
| 实验步骤 | 实验现象与结论 |

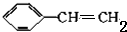 .
.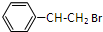 ;
;
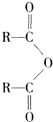 $\stackrel{H_{2}O}{→}$2RCOOH ②RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH
$\stackrel{H_{2}O}{→}$2RCOOH ②RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH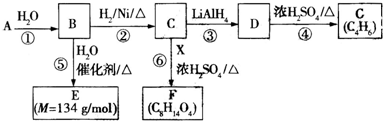
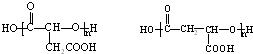 (一种即可).
(一种即可).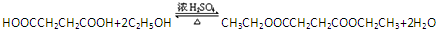 .
. .Y与足量氢氧化钠溶液反应所得产物之一M,能与灼热的氧化铜反应,写出M与灼热的氧化铜反应的化学方程式:
.Y与足量氢氧化钠溶液反应所得产物之一M,能与灼热的氧化铜反应,写出M与灼热的氧化铜反应的化学方程式: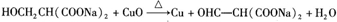 .
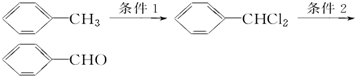
.
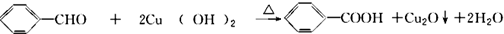 .
.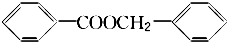 .
.