题目内容
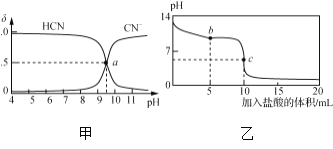
【题目】25 ℃时,NaCN溶液中CN-、HCN浓度所占分数(δ)随pH变化的关系如下图甲所示。向10 mL 0.01 mol·L-1 NaCN溶液中逐滴加入0.01 mol·L-1的盐酸,其pH变化曲线如下图乙所示。
下列溶液中微粒的物质的量浓度关系一定正确的是( )
A. 图甲中pH=7的溶液:c(Cl-)=c(HCN)
B. 图甲中a点的溶液:c(CN-)<c(Cl-)
C. 图乙中b点的溶液:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+)
D. 图乙中c点的溶液:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-)
【答案】AD
【解析】
A. 由图可知,图甲中pH=7时,c(HCN)>c(CN-),而根据电荷守恒可以知道,c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(CN-),由于c(H+)=c(OH-),则c(Na+)=c(Cl-)+c(CN-),根据物料守恒得c(Na+)= c(HCN)+ c(CN-),所以c(Cl-)=c(HCN),故A正确;
B. 图甲中的a点是HCN、CN-浓度相等,根据物料守恒得c(Na+)= c(HCN)+ c(CN-),而根据电荷守恒可以知道,c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(CN-),则 c(HCN)+c(H+)=c(OH-)+c(Cl-),由图可知,此时溶液pH>7,c(H+)<c(OH-),所以c(CN-)=c(HCN)>c(Cl-),故B错误;
C. 图乙中b点时,溶液中溶质为等物质的量浓度的溶液:c(NaCN)=c(NaCl)=c(HCN),溶液呈碱性,说明CN-的水解程度大于HCN的电离程度,所以c(HCN)> c(Cl-)> c(CN-)> c(OH-)> c(H+),故C错误;
D. 图乙中c点的溶液,二者恰好完全反应,根据物料守恒得c(Cl-)= c(Na+)= c(HCN)+ c(CN-),而根据电荷守恒可以知道,c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(CN-),则c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-),所以D选项是正确的。
答案选AD。

【题目】烟气(主要污染物SO2、NOX)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中的SO2、NOx 的含量。
(1) O3氧化烟气中SO2、NOx 的主要反应的热化学方程式为: NO(g)+O3(g)![]() NO2(g)+ O2(g) ΔH=-200.9 kJ·mol-13NO(g)+O3(g)
NO2(g)+ O2(g) ΔH=-200.9 kJ·mol-13NO(g)+O3(g)![]() 3NO2(g) ΔH=-317.3kJ·mol-1。则2NO2(g)
3NO2(g) ΔH=-317.3kJ·mol-1。则2NO2(g)![]() 2NO(g)+O2(g)的ΔH=_____________kJ·mol-1
2NO(g)+O2(g)的ΔH=_____________kJ·mol-1
(2)T℃时,利用测压法在刚性反应器中,投入一定量的NO2发生反应3NO2(g)![]() 3NO(g)+O3(g),体系的总压强 p随时间 t的变化如下表所示:
3NO(g)+O3(g),体系的总压强 p随时间 t的变化如下表所示:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
压强/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
①若降低反应温度,则平衡后体系压强 p______24.00 MPa(填“>”、“<”或“=”),原因是____________。
②15min 时,反应物的转化率 α=______。
③T℃时反应3NO2(g)![]() 3NO(g)+O3(g)的平衡常数Kp=____________(Kp 为以分压表示的平衡常数,分压等于总压乘以该气体的物质的量分数)
3NO(g)+O3(g)的平衡常数Kp=____________(Kp 为以分压表示的平衡常数,分压等于总压乘以该气体的物质的量分数)
(3)T℃时,在体积为2L的密闭刚性容器中,投入2 mol NO2发生反应2NO2(g)![]() 2NO(g)+O2(g),实验测得:v正=k正 c2(NO2),v逆=k逆 c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为T℃时NO2的转化率随时间变化的结果如图所示(反应在5.5min时达到平衡):
2NO(g)+O2(g),实验测得:v正=k正 c2(NO2),v逆=k逆 c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为T℃时NO2的转化率随时间变化的结果如图所示(反应在5.5min时达到平衡):

①在体积不变的刚性容器中,投入固定量的NO2发生反应,要提高NO2转化率,可采取的措施是______________、___________。
②由图中数据,求出该反应的平衡常数为_________。
③计算A 点处v正/v逆=_________________________(保留1位小数)。