题目内容
【题目】下列说法正确的是( )
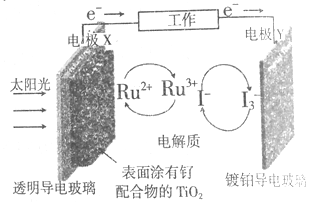
A. 甲醇燃料电池工作时,甲醇得到电子,发生还原反应
B. 室温下,稀释0.1 mol·L-1氨水,c(H+)·c(NH3·H2O)的值减小
C. 将1 mol Cl2通入水中,HClO、Cl-、ClO-粒子数之和为2×6.02×1023
D. SiO2(s)+2C(s)===Si(s)+2CO(g)在常温下不能自发进行,则该反应的ΔH<0
【答案】B
【解析】
A. 甲醇燃料电池中,通入甲醇的电极是负极,负极上失电子发生氧化反应,故A错误;
B. 由NH3H2OOH-+NH4+可知,加水促进电离,因温度不变,则电离平衡常数不变,水的离子积也不变,Kb=![]() =
=![]() ,由于c(H+)和c(OH-)的乘积不变,而c(NH4+)减小,则c(H+)·c(NH3·H2O)的值减小,故B正确;
,由于c(H+)和c(OH-)的乘积不变,而c(NH4+)减小,则c(H+)·c(NH3·H2O)的值减小,故B正确;
C. 氯气和水的反应为可逆反应,不能进行彻底,故氯水中含未反应的氯气分子,即溶液中的HClO、Cl-、ClO-粒子数之和小于2×6.02×1023,故C错误;
D. △H-T△S>0,反应非自发进行,反应△S>0,满足△H-T△S>0,则△H>0,故D错误。
答案选B。

练习册系列答案
相关题目