题目内容
【题目】一定条件下向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体,图 1 表示各物质浓度随时间的变化,图 2 表示速率随时间的变化,t2、t3、t4、t5 时刻各改变一种条件,且改变的条件均不同。若t4时刻 改变的条件是压强,则下列说法错误的是

A.若 t1=15 s,则前 15 s 的平均反应速率 v(C)=0.004 mol·L-1·s-1
B.该反应的化学方程式为 3A(g)![]() B(g)+2C(g)
B(g)+2C(g)
C.t2、t3、t5 时刻改变的条件分别是升高温度、加入催化剂、增大反应物浓度
D.若 t1=15 s,则 B 的起始物质的量为 0.04 mol
【答案】C
【解析】
A. 反应在t1时刻达到平衡时,气体C的浓度增大0.06mol·L-1,所以平均反应速率为v(C)= ![]() =0.004 mol·L-1·s-1,故A正确;
=0.004 mol·L-1·s-1,故A正确;
B. t4时刻降低压强后反应平衡状态没有改变,说明反应物系数和与生成物系数和相等,又因为反应第一次达到平衡时气体A浓度降低0.09mol·L-1,气体C的浓度增大0.06 mol·L-1,所以气体A与C的系数比为3:2,因此气体B也是生成物且其系数为1,所以化学方程式为3A(g)B(g)+2C(g),故B正确;
C. t5时刻后若为增大反应物浓度,开始时应该只有正反应速率增大,不会两个反应速率同时增大,故C错误;
D. 气体C的浓度增大0.06mol·L-1,气体B、C的反应系数比为1:2,所以气体B浓度增大0.03mol·L-1,又由初始气体A浓度可知,容器的体积为0.3mol/0.15molL1=2L,可知气体B起始物质的量为(0.05-0.03)mol·L-1×2L=0.04mol,故D正确;
答案选C。

【题目】N2O俗名为“笑气”,也是一种温室气体。结合所学知识,回答下列问题:
(1)锌与极稀硝酸反应可生成N2O,该反应的化学方程式为___________,其中作氧化剂的硝酸与参与反应的硝酸的物质的量之比为___________。
(2)已知几种物质的相对能量如下:
物质 | N2O(g) | CO(g) | N2(g) | CO2(g) |
相对能量/kJmol-1 | 475.5 | 283.0 | 393.5 | 0 |
①N2O(g)和CO(g)反应生成N2(g)和CO2(g)的热化学方程式为____________。
②若其他条件不变,加入高效催化剂,该反应的焓变将_______(填“增大”、“减小”或“不变”)。
(3)碘蒸气能催化N2O的分解,反应历程(步骤)如下:
i.I2(g)2I(g)
ii.I(g)+N2O(g)=N2(g)+IO(g)
iii.2IO(g)+2N2O(g)=2N2(g)+2O2(g)+I2(g)
实验表明,在反应过程c(I)始终大于c(IO),由此推测,反应速率ii_________iii(填“>”、“<”或“=”)。
(4)一定温度下,向恒容密闭容器中充入2 mol N2O(g)和3 mol NO(g),发生反应:N2O(g)+NO(g)N2(g)+NO2(g) △H。测得N2体积分数与温度、时间的关系如图所示。
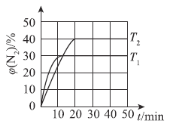
①△H___________0(填“>”、“<”或“=”)。
②下列情况表明该反应达到平衡状态的是___________(填字母)。
A.混合气体的密度不再改变 B.相对分子质量不再改变
C.NO和NO2的消耗速率相等 D.N2O的体积分数不再改变
③T1时,该反应的平衡常数K=___________。
【题目】某校化学研究小组会试对校园附近空气质量进行测定请回答下列问题。
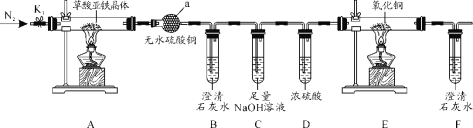
(1)甲组同学设计了如图所示的实验装置,对空气中SO2、悬浮颗粒物含量进行测定。下列装置连接的顺序为(填序号 )________________。

注:气体流速管是用来测量单位时间内通过气体的体积的装置
①用上述装置定量测定空气中的SO2和可吸入颗粒的含量,除测定气体流速(单位:cm3·min-1)外还需要测定____________、____________。
②已知:碘单质微溶于水,KI可以增大碘在水中的溶解度。请你协助甲组同学完成100mL 5×10-4mo1 L-1碘溶液的配制:
第一步:用电子天平准确称取1.27g碘单质加入烧杯中,______________。
第二步:将第一步所得溶液和洗涤液全部转入_____ mL的容量瓶中,加水定容,摇匀。
第三步:从第二步所得溶液中取出10.00mL溶液倒入100mL容量瓶中,加水稀释至刻度线,摇匀。
(2)乙组同学拟用如图简易装置测定空气中的SO2含量:

①检查该装置的气密性时,先在试管中装入适量的水(保证玻璃管的下端浸没在水中)。然后__________(填写操作方法)时。将会看到_____________(填写实验现象),则证明该装置的气密性良好。
②测定指定地点空气中的SO2含量准确移取1.00mL 5×10-4mo1L-1碘溶液,注入如图所示试管中。用适量的蒸馏水桸释后,再加2~3滴淀粉溶液,配制成溶液A。甲、乙两组同学分别使用如图所示相同的实验装置和溶液A,在同一地点、同时推拉注射器的活塞,反复抽气,直到溶液的蓝色全部褪尽为止停止抽气,记录抽气次数如下(假设每次抽气500mL)。
分组 | 甲组 | 乙组 |
抽气次数 | 110 | 145 |
我国环境空气质量标准对空气质量测定中SO2的最高浓度限值如下表:
最高浓度限值/mg·m-3 | ||
一级标准 | 二级标准 | 三级标准 |
0.15 | 0.50 | 0. 70 |
经老师和同学们分析,判断甲组测定结果更为准确,则该地点的空气中SO2 的含量为_______mgm-3(保留2 位有效数字),属于________(填汉字)级标准;请你分析乙组实验结果产生较大偏差的原因是(两个小组所用装置和药品均无问题)______________。