题目内容
【题目】在一定条件下,反应A(g)+B(g)C(g)△H<0,达平衡后,在下列空格填入对应图的序号:
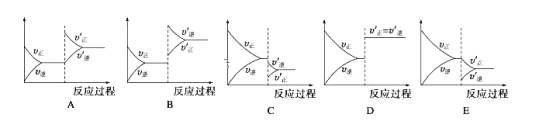
(1)升温:______
(2)减压:______
(3)减少C的量:______
(4)增加A的量:______
(5)使用催化剂:______.
【答案】B C E A D
【解析】
(1)升温,化学反应速率加快,反应向着吸热方向进行;
(2)减压,正逆反应速率减慢,反应向着气体系数和增加的方向进行;
(3)减少C的量:正逆反应速率减慢,但是平衡正向移动,所以正反应速率大于逆反应速率;
(4)增加A的量:正逆反应速率加快,但是平衡正向移动,所以正反应速率大于逆反应速率;
(5)使用催化剂:正逆反应速率都加快,但是不会引起化学平衡的移动.
(1)升温,正逆化学反应速率迅速加快,反应向着吸热方向进行,即向着逆向进行,所以逆反应速率大于正反应速率,故选B;
(2)减压,正逆反应速率都减慢,反应向着气体系数和增加的方向即逆向进行,所以逆反应速率大于正反应速率,故选C;
(3)减少C的量:正逆反应速率减慢,逆反应速率迅速减慢,但是平衡正向移动,所以正反应速率大于逆反应速率,故选E;
(4)增加A的量:正逆反应速率加快,但是平衡正向移动,所以正反应速率大于逆反应速率,故选A;
(5)使用催化剂:正逆反应速率都加快,但是不会引起化学平衡的移动,故选D.

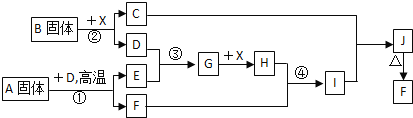
【题目】已知海水提取镁的主要步骤如下:
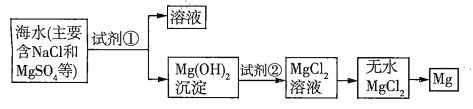
(1)关于加入试剂①作沉淀剂,有以下方法,请完成下列问题。
方法 | 是否合理 | 简述理由 |
方法:高温加热蒸发海水后,再加入沉淀剂 | a | b |
你认为合理的其他方法是c |
a. _____________;
b.____________;
c.____________。
(2)框图中加入的试剂①应该是_______(填物质名称),加入试剂②的溶质是_______(填化学式)。工业上由无水![]() 制取镁的化学方程式为___________。
制取镁的化学方程式为___________。