题目内容
12.某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验内容如图: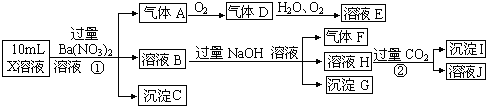
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是Al3+、NH4+、Fe2+、SO42-,不能确定是否含有的离子是Fe3+、Cl-,若要确定不能确定的离子中阴离子不存在,检验的最可靠的化学方法是用试管取少量X溶液,加入足量硝酸钡溶液,静置取上层清夜,滴加AgNO3溶液,无白色沉淀说明无Cl-
(2)写出有关离子方程式:①中生成A3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.②AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
(3)假设测定A、F、I均为0.01mol,10mL X溶液中n(H+)=0.02mol,当沉淀C物质的量为>0.06mol,表明不能确定的离子中阳离子一定存在.
分析 在强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定的是否含有的离子Fe3+和Cl-,以此解答(1)(2)题,根据溶液电中性解答(3)题.
解答 解:(1)在强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaOH和NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,检验氯离子的方法是:取少量B溶液放在试管中,加入几滴AgNO3溶液,无白色沉淀说明无Cl-,
故答案为:Al3+、NH4+、Fe2+、SO42-;Fe3+、Cl-;用试管取少量X溶液,加入足量硝酸钡溶液,静置取上层清夜,滴加AgNO3溶液,无白色沉淀说明无Cl-;
(2)①Fe2+离子被氧化为Fe3+离子,反应的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;②H为NaOH和NaAlO2混合物,通入过量二氧化碳后分别发生的反应为:CO2+OH-=HCO3-,AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;CO2+OH-=HCO3-,AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(3)A、F、I均为0.01mol,10mL X溶液中n(H+)=0.02mol,根据反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,可知3Fe2+离子为0.03mol,根据溶液电中性可知:2n(Fe2+)+3n(Al3+)+n(NH4+)+n(H+)=2n(SO42-),n(SO42-)=$\frac{2×0.03mol+3×0.01mol+0.01mol+0.02mol}{2}$=0.06mol,当沉淀C物质的量>0.06mol时一定含有Fe3+离子,故答案为:>0.06.
点评 本题为考查离子组推断题,题目具有一定难度,本题解答时一定要紧扣反应现象,推断各离子存在的可能性,本题易错点为(3)题,注意溶液电中性的利用.

 小学课时特训系列答案
小学课时特训系列答案| A. | 光导纤维、防弹玻璃、氧化铝陶瓷、硅藻土都是无机非金属材料,PLA、PE、橡胶、酚醛树脂都是人工合成高分子材料 | |
| B. | 贮氢金属并不是简单地吸附氢气,而是通过化学反应贮存氢气 | |
| C. | 科学家发现一种新的CO2晶体,该CO2晶体具有极强的硬度,是由CO2分子构成的空间立体网状结构 | |
| D. | 最新的氯碱工业是用离子交换膜电解槽电解饱和食盐水来生产氢气、氯气和烧碱的,电解槽中的离子交换膜既可以用阳离子交换膜也可以用阴离子交换膜 |
| A. | 丙烯分子中有8个σ键,1个π键 | |
| B. | 在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 | |
| C. | NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力 | |
| D. | NCl3和BC13分子中,中心原子都采用sp3杂化 | |
| E. | 在“冰→水→水蒸气→氧气和氢气”的变化过程中,各阶段被破坏的粒子间主要的相互作用依次是氢键、分子间作用力、极性键 |
| A. | 78 gNa2O2晶体中所含阴阳离子个数均为2NA | |
| B. | 1.5 g CH3+中含有的电子数为NA | |
| C. | 3.4 g氨气分子中含有0.6NA个N-H键 | |
| D. | 常温下,100 mL1 mol•L-1AlCl3溶液中Al3+离子总数等于0.1NA |
| 编号 | A | B | C | D |
实验 装置 | 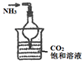 | 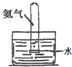 | 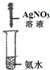 | 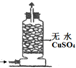 |
| 实验 目的 | 实验室模拟侯氏制碱法制备NH4HCO3 | 验证NH3易溶于水 | 制备银氨溶液 | 干燥NH3 |
| A. | 0.4mol | B. | 0.3 mol | C. | 0.2mol | D. | 0.1 mol |