题目内容
如下图是常见仪器的部分结构。
(1)写出仪器名称A ,B ,C ,D 。
(2)使用前需检查是否漏水的仪器有 。
(1)量筒 容量瓶 滴定管 温度计
(2)BC
解析

 小夫子全能检测系列答案
小夫子全能检测系列答案下列有关实验操作的叙述正确的是
| A.用过滤法分离氢氧化铁胶体和三氯化铁溶液的混合物 |
| B.将5.85gNaCl固体溶于1000mL容量瓶中,加水定容后即可制得0.1mol?L-1的NaCl溶液 |
| C.向含有少量Ca(OH)2的Mg(OH)2悬浊液中加入饱和MgCl2溶液,充分搅拌后过滤,洗涤,可达到除去Mg(OH)2中的少量Ca(OH)2的目的 |
| D.精炼铜时,粗铜做阴极,纯铜做阳极,电解质溶液为CuSO4溶液 |
下列实验操作正确的是
| A.盛放NaOH溶液时,使用带玻璃塞的磨口瓶 |
| B.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| C.NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
| D.做“钠与水的反应”实验时,切取绿豆大小的金属钠,用滤纸吸干其表面的煤油,放入烧杯中,滴入两滴酚酞溶液,再加入少量水,然后观察并记录实验现象 |
下列关于研究物质性质的基本程序,排列顺序正确是( )
a观察物质的外观性质,b实验和观察,c解释及结论,d预测物质的性质
| A.bacd | B.abcd | C.adbc | D.dabc |
下列叙述正确的是( )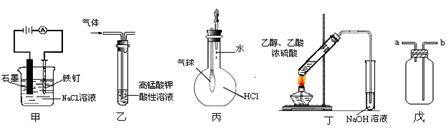
①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊既可用于收集H2、CO2、Cl2和HCl气体,也可用于干燥H2、CO2、Cl2和HCl气体。
| A.①⑤ | B.④⑤ | C.①② | D.③⑤ |
有关钴和铁化合物的性质见下表:
| 化学式 | 溶度积(室温时)Ksp | 沉淀完全时的pH | 氯化钴晶体的性质 |
| Co(OH) 2 | 5.9×10-15 | 9.4 | CoCl2·6H2O呈红色,常温下稳定。110ºC~120ºC时脱水变成蓝色无水氯化钴 |
| Fe(OH) 2 | 1.6×10-14 | 9.6 | |
| Fe(OH) 3 | 1.0×10-35 | x |
用含钴废料(含少量铁)可制备氯化钴:Co+2HCl=CoCl2+H2↑工艺流程如下:

试回答:
(1)“净化除铁”中,写出加入CoCO3(难溶)调pH时反应的离子方程式
(2)滤液中(Fe3+)≤1.0×10-5mol/L时,可视为Fe3+沉淀完全。试计算室温下,Fe(OH) 3沉淀完全时,则x= 。
(3)②步中用CoCO3调pH略大于x的原因是 。
(4)滤液中所含溶质有 , 。
(5)为了防止CoCl2·6H2O脱水,“干燥”时宜采用的方法或操作是 , 。
(12分)为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)实验过程如下:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中的溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
V.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子.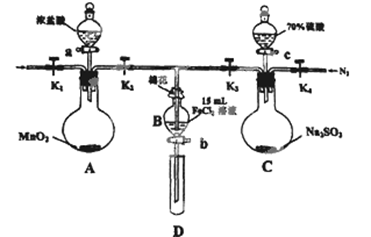
(1)过程Ⅰ的目的是______________________。
(2)棉花中浸润的溶液为__________________。
(3)A中发生反应的化学方程式为__________________________________。
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是______________
(5)过程Ⅵ中检验B溶液中是否含有硫酸根的操作是________________________________
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| | 过程IV B溶液中含有的离子 | 过程VI B溶液中含有的离子 |
| 甲 | 有Fe3+无Fe2+ | 有SO42﹣ |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42﹣ |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |