题目内容
4.下列有关氨及氨水的说法中,正确的是( )| A. | NH3是10电子分子,具有还原性 | B. | 液氨、氨气、氨水是同一种物质 | ||
| C. | 氨气是非电解质,氨水是电解质 | D. | NH3•H2O是混合物 |
分析 A、氨气是10电子的微粒,N元素处于最低价,具有还原性;
B、氨水是氨气溶于水形成的混合物,氨气与液氨是一种物质,只是状态不同;
C、氨水是混合物,既不是电解质也不是非电解质;
D、一水合氨是纯净物,属于碱.
解答 解:A、氨气中电子数为1×3+7=10,故是10电子的微粒,N元素处于最低价,具有还原性,故A正确;
B、氨水是氨气溶于水形成的混合物,氨气与液氨是一种物质,只是状态不同,故此三者中氨水与其余二者不是同种物质,故B错误;
C、氨水是混合物,既不是电解质也不是非电解质,故C错误;
D、一水合氨是纯净物,属于弱碱,故D错误,故选A.
点评 本题以氨水为载体考查了基本概念,知道氨水呈碱性的原因,明确氨水中存在的微粒,再结合基本概念来分析解答,题目难度不大.

练习册系列答案
相关题目
14.下列判断正确的是( )
| A. | 通入足量CO2后的溶液中大量共存:Na+、SiO32-、CH3COO-、CO32- | |
| B. | pH=9的CH3COONa溶液和pH=9的NH3•H2O溶液,两溶液中水的电离程度相同 | |
| C. | NH4Al(SO4)2溶液中滴加足量的NaOH的离子方程式为:NH4++Al3++5OH-=NH3•H2O+AlO2-+2H2O | |
| D. | Fe2+、SO2都能使酸性高锰酸钾溶液褪色,前者表现出还原性,后者表现出漂白性 |
15.下列说法正确的是( )
| A. | NaHSO4溶液中,c(Na+)+c(H+)=c(SO42-)+c(OH-) | |
| B. | 室温时水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量共存 | |
| C. | 等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3中c(CO32-)的大小关系为:②>④>③>① | |
| D. | 在明矾溶液中加入氢氧化钡溶液至沉淀的质量达到最大值时发生反应的离子方程式:2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓ |
12.下列分子式表示的物质,没有同分异构体的是( )
| A. | C4H8 | B. | C4H10 | C. | C3H6 | D. | C2H4 |
9.有专家指出,如果将燃烧产物如CO2、H2O、N2等利用太阳能使它们重新变成CH4、CH3OH、NH3等的构想能够成为现实,则下列说法中,错误的是( )
| A. | 可消除对大气的污染 | |
| B. | 可节约燃料 | |
| C. | 可缓解能源危机 | |
| D. | 此题中的CH4、CH3OH、NH3等为一级能源 |
16.下列关于乙酸与乙醇的说法正确的是( )
| A. | 互为同分异构体 | B. | 都能氧化为乙醛 | ||
| C. | 水溶液均显酸性 | D. | 可用石蕊溶液加入鉴别 |
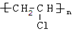 ,反应类型为加聚反应.
,反应类型为加聚反应.