题目内容
9.有专家指出,如果将燃烧产物如CO2、H2O、N2等利用太阳能使它们重新变成CH4、CH3OH、NH3等的构想能够成为现实,则下列说法中,错误的是( )| A. | 可消除对大气的污染 | |
| B. | 可节约燃料 | |
| C. | 可缓解能源危机 | |
| D. | 此题中的CH4、CH3OH、NH3等为一级能源 |
分析 根据太阳能将CO2、H2O、N2等气体重新组合成燃料,燃料燃烧又生成CO2、H2O、N2等,利用太阳能将之循环使用,结合能源危机及大气污染判断.
解答 解:在此构想的物质循环中,太阳能将CO2、H2O、N2等气体重新组合成燃料,此过程为太阳能→化学能;燃料燃烧,化学能→热能,故在此构想的物质循环中太阳能最终转化为热能,即可消除对大气的污染,又节约燃料缓解能源危机,故ABC都正确;CH4、CH3OH、NH3等为二级能源,故D错误.
故选:D.
点评 本题主要考查能量之间的相互转化,关注能源危机及大气污染物的排放即可解题,难度不大.

练习册系列答案
相关题目
19.下列解释事实的方程式不正确的是( )
| A. | 铝热法炼铁:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | |
| B. | 工业进行“氮的固定”:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 | |
| C. | 铅蓄电池充电时阴极反应:PbSO4(s)+2e-=Pb(s)+SO42-(aq) | |
| D. | 用铜和稀硝酸制备硝酸铜:Cu+4H++2NO3-=Cu2++2NO2↑+2H2 |
20.国务院颁布的《“十二五”控制温室气体排放工作方案》提出,2015年我国单位国内生产总值CO2排放要比2010年下降17%.下列说法不正确的是( )
| A. | CO2属于酸性氧化物 | |
| B. | CO2是导致酸雨发生的主要原因 | |
| C. | 可用Na2CO3溶液捕捉(吸收)CO2 | |
| D. | 使用氢能源替代化石燃料可减少CO2排放 |
4.下列有关氨及氨水的说法中,正确的是( )
| A. | NH3是10电子分子,具有还原性 | B. | 液氨、氨气、氨水是同一种物质 | ||
| C. | 氨气是非电解质,氨水是电解质 | D. | NH3•H2O是混合物 |
14.某溶液中大量存在Ba2+、H+、Cl-,该溶液中还可能大量存在的离子是( )
| A. | Ag+ | B. | SO42- | C. | CH3COO- | D. | Mg2+ |
1.下列离子方程式书写不正确的是( )
| A. | 常温下氯气与烧碱溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | AlCl3溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 金属钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 铜与稀硝酸反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
18.下列做法或实验操作正确的是( )
| A. | 振荡分液漏斗时应关闭其玻璃塞和活塞 | |
| B. | 用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2 | |
| C. | 在50mL量筒中配制0.1000mol•L-1碳酸钠溶液 | |
| D. | 检验NH4+时,向试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 |
9.金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”.以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如图1:

回答下列问题:
(1)钛铁矿和浓硫酸反应的产物之一是TiOSO4,反应中无气体生成.副产品甲阳离子是Fe2+.
(2)上述生产流程中加入铁屑的目的是防止Fe2+氧化.
(3)此时溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子.常温下,其对应氢氧化物的Ksp如下表所示.
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol•L-1,当溶液的pH等于10时,Mg(OH)2开始沉淀.
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,写出该反应的离子方程式:TiO2++2H2O═H2TiO3↓+2H+.
(4)Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是隔绝空气.
(5)在800~1000℃时电解TiO2也可制得海绵钛,装置如图2所示.图中b是电源的正极,阴极的电极反应式TiO2+4e-═Ti+2O2-.

回答下列问题:
(1)钛铁矿和浓硫酸反应的产物之一是TiOSO4,反应中无气体生成.副产品甲阳离子是Fe2+.
(2)上述生产流程中加入铁屑的目的是防止Fe2+氧化.
(3)此时溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子.常温下,其对应氢氧化物的Ksp如下表所示.
| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,写出该反应的离子方程式:TiO2++2H2O═H2TiO3↓+2H+.
(4)Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是隔绝空气.
(5)在800~1000℃时电解TiO2也可制得海绵钛,装置如图2所示.图中b是电源的正极,阴极的电极反应式TiO2+4e-═Ti+2O2-.
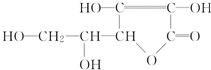 维生素C的结构简式如图所示:
维生素C的结构简式如图所示: