题目内容
16.下列关于乙酸与乙醇的说法正确的是( )| A. | 互为同分异构体 | B. | 都能氧化为乙醛 | ||
| C. | 水溶液均显酸性 | D. | 可用石蕊溶液加入鉴别 |
分析 A、分子式相同,结构不同的互称为同分异构体;
B、乙酸不具备还原性,不能氧化生成乙醛;
C、乙醇不能电离;
D、乙酸能电离出氢离子,使石蕊溶液显红色,乙醇不能使石蕊溶液变色.
解答 解:A、乙醇分子式为C2H6O,乙酸分子式为C2H4O2,二者分子式不同,不是同分异构体,故A错误;
B、乙酸不能被氧化生成乙醛,故B错误;
C、乙醇不能电离出自由移动的氢离子,无酸性,故C错误;
D、乙酸能电离出氢离子,使石蕊溶液显红色,乙醇不能使石蕊溶液变色,故可以利用石蕊溶液鉴别乙醇和乙酸,故D正确,故选D.
点评 本题主要考查的是乙醇与乙酸的性质以及鉴别,掌握乙醇中羟基的性质是关键,难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
6.已知某强酸性的溶液中存在大量的NO3-,下列有关该溶液中还存在的物质叙述正确的是( )
| A. | 铝元素能以Al3+或AlO2-的形式存在 | |
| B. | 铁元素能以Fe2+和Fe3+的形式共存 | |
| C. | 硫元素主要以SO42-的形式存在 | |
| D. | 氯元素能以Cl-或ClO-的形式存在 |
7.图象能直观地反映有关物理量的变化及规律,下列各图象与描述相符的是( )
| A. | 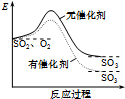 如图表示SO2氧化反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| B. | 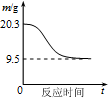 如图表示0.1 mol MgCl2•6H2O在空气中充分加热时固体质量随时间的变化 | |
| C. | 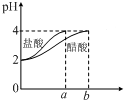 如图表示分别稀释10 mL pH=2的盐酸和醋酸时溶液pH的变化,图中b>100 | |
| D. | 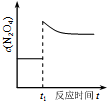 如图表示平衡2NO2(g)?N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 |
4.下列有关氨及氨水的说法中,正确的是( )
| A. | NH3是10电子分子,具有还原性 | B. | 液氨、氨气、氨水是同一种物质 | ||
| C. | 氨气是非电解质,氨水是电解质 | D. | NH3•H2O是混合物 |
11.我国宣布到2030年非化石能源占一次能源消费比重将提高到20%左右.下列不属于化石能源的是( )
| A. | 煤 | B. | 石油 | C. | 天然气 | D. | 生物质能 |
1.下列离子方程式书写不正确的是( )
| A. | 常温下氯气与烧碱溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | AlCl3溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 金属钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 铜与稀硝酸反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
8.对于元素周期表中下列位置的①~⑩十种元素,请回答有关问题.(用元素符号或化学式回答)
(1)能形成共价键的元素有H、C、N、O、F、S、Cl元素.
(2)只需形成一个共价单键就能达到稳定结构的元素有H、F、Cl.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ||||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
(2)只需形成一个共价单键就能达到稳定结构的元素有H、F、Cl.
5.在容积一定的密闭容器中,反应2A?B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是( )
| A. | 正反应是吸热反应,且A不是气态 | B. | 正反应是放热反应,且A不是气态 | ||
| C. | 正反应是吸热反应,且A是气态 | D. | 正反应是放反应,且A是气态 |
16.下列关于有机化合物的说法完全正确的是( )
| A. | 只有在生物体内才能合成的物质 | B. | 有机物都是含有碳元素的化合物 | ||
| C. | 有机化合物都能燃烧 | D. | 含有碳元素的物质 |