题目内容
3.去甲肾上腺素可以调控动物机体的植物性神经功能,其结构简式如图所示.下列说法正确的是( )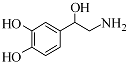
| A. | 每个去甲肾上腺素分子中含有3个酚羟基 | |
| B. | 每个去甲肾上腺素分子中含有2个手性碳原子 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
分析 该分子中含有酚羟基、醇羟基、氨基和苯环,具有酚、醇、胺及苯的性质,能发生取代反应、氧化反应、还原反应、加成反应、取代反应等,连接四个不同原子或原子团的碳原子属于手性碳原子,据此分析解答.
解答 解:A.只有直接连接苯环的羟基才是酚羟基,所以该分子中含2个酚羟基、1个醇羟基,故A错误;
B.该分子中只有连接醇羟基的碳原子为手性碳原子,所以只有一个手性碳原子,故B错误;
C.苯环上酚羟基邻对位氢原子能被溴取代,且以1:1所以,所以1mol去甲肾上腺素最多能与3molBr2发生取代反应,故C错误;
D.含有酚羟基,具有酸性,含有氨基,具有碱性,所以去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系即可解答,侧重考查酚、醇和胺的性质,注意苯环上酚羟基邻对位氢原子才能和溴原子发生取代反应,注意酚羟基和醇羟基的区别,易错选项是B.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
6.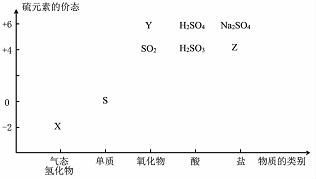 物质的类别和核心元素的化合价是研究物质性质的两个基本视角?
物质的类别和核心元素的化合价是研究物质性质的两个基本视角?
(1)图中X的电子式为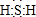 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱 (填“强”或“弱”)?用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱?
;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱 (填“强”或“弱”)?用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱?
(2)Na2S2O3是一种用途广泛的钠盐?
①下列物质用于Na2S2O3的制备,从氧化还原反应的角度,理论上有可能的是bd (填字母序号)?
a.Na2S+S b.Z+S c.Na2SO3+Y d.NaHS+NaHSO3
②已知反应:Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O?研究其反应速率时,下列说法正确的是b(填写字母序号)?
a.可通过测定一段时间内生成SO2的体积,得出该反应的速率
b.可通过比较出现浑浊的时间,研究浓度?温度等因素对该反应速率的影响
c.可通过Na2S2O3固体与稀硫酸和浓硫酸的反应,研究浓度对该反应速率的影响
(3)治理含CO?SO2的烟道气,可以将其在催化剂作用下转化为单质S和无毒的气体?
①已知:CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283kJ•mol-1
S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1
则治理烟道气反应的热化学方程式为2CO(g)+SO2 (g)═S(s)+2CO2(g)△H=-270 kJ•mol-1?
②一定条件下,将CO与SO2以体积比为4:1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是cd (填写字母序号)?
a.v(CO):v(SO2)=2:1
b.平衡常数不变
c.气体密度不变
d.CO2和SO2的体积比保持不变
测得上述反应达平衡时,混合气体中CO的体积分数为$\frac{7}{11}$,则SO2的转化率为60%?
(4)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇?甲醇可制作燃料电池?写出以氢氧化钾为电解质的甲醇燃料电池负极反应式CH3OH-6e-+8OH-=CO32-+6H2O?
(5)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表?
吸收CO2最合适的试剂是Ba(OH)2 (填“Ca(OH)2”或“Ba(OH)2”)溶液?
 物质的类别和核心元素的化合价是研究物质性质的两个基本视角?
物质的类别和核心元素的化合价是研究物质性质的两个基本视角?(1)图中X的电子式为
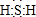 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱 (填“强”或“弱”)?用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱?
;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱 (填“强”或“弱”)?用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱?(2)Na2S2O3是一种用途广泛的钠盐?
①下列物质用于Na2S2O3的制备,从氧化还原反应的角度,理论上有可能的是bd (填字母序号)?
a.Na2S+S b.Z+S c.Na2SO3+Y d.NaHS+NaHSO3
②已知反应:Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O?研究其反应速率时,下列说法正确的是b(填写字母序号)?
a.可通过测定一段时间内生成SO2的体积,得出该反应的速率
b.可通过比较出现浑浊的时间,研究浓度?温度等因素对该反应速率的影响
c.可通过Na2S2O3固体与稀硫酸和浓硫酸的反应,研究浓度对该反应速率的影响
(3)治理含CO?SO2的烟道气,可以将其在催化剂作用下转化为单质S和无毒的气体?
①已知:CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283kJ•mol-1
S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1
则治理烟道气反应的热化学方程式为2CO(g)+SO2 (g)═S(s)+2CO2(g)△H=-270 kJ•mol-1?
②一定条件下,将CO与SO2以体积比为4:1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是cd (填写字母序号)?
a.v(CO):v(SO2)=2:1
b.平衡常数不变
c.气体密度不变
d.CO2和SO2的体积比保持不变
测得上述反应达平衡时,混合气体中CO的体积分数为$\frac{7}{11}$,则SO2的转化率为60%?
(4)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇?甲醇可制作燃料电池?写出以氢氧化钾为电解质的甲醇燃料电池负极反应式CH3OH-6e-+8OH-=CO32-+6H2O?
(5)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表?
| 溶解度(s)/g | 溶度积(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
18.下列说法正确的是( )
①H、2H、3H为三种不同的核素;
②H、2H、3H互为同位素;
③H、2H、3H互为同素异形体;
④114号元素位于周期表第七周期VA族;
⑤氢元素质量数为1;
⑥同位素的“同位”指核素的质子数相同,在元素周期表中占相同的位置;
⑦互为同位素的原子物理性质、化学性质均相同.
①H、2H、3H为三种不同的核素;
②H、2H、3H互为同位素;
③H、2H、3H互为同素异形体;
④114号元素位于周期表第七周期VA族;
⑤氢元素质量数为1;
⑥同位素的“同位”指核素的质子数相同,在元素周期表中占相同的位置;
⑦互为同位素的原子物理性质、化学性质均相同.
| A. | ①②⑥⑦ | B. | ①②③⑥ | C. | ①②⑥ | D. | ①②③⑥⑦ |
12.下列说法中正确的是( )
| A. | 乙烯中C=C的键能是乙烷中C-C的键能的2倍 | |
| B. | 同一原子中,2p,3p,4p能级的轨道数目依次增多 | |
| C. | C-O键的极性比N-O键的极性大 | |
| D. | 根据能量最低原理,原子的核外电子排布先填满离核近的轨道,再填充离核远的轨道 |
 .
. .
. 的系统命名法的名称为2,2,5,5-四甲基庚烷.
的系统命名法的名称为2,2,5,5-四甲基庚烷. 某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述正确的是( )
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述正确的是( )