题目内容
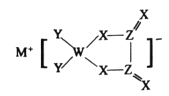
【题目】已知:P4(g)+6Cl2(g)=4PCl3(g) ΔH=a kJ·mol-1,Cl—Cl键的键能为bkJ·mol-1,PCl3中P—Cl键的键能为ckJ·mol-1,P4的结构为![]() 。则P—P键的键能为
。则P—P键的键能为
A.(a-6b+12c)/6kJ·mol-1B.(a-3b+12c)/4kJ·mol-1
C.(a-6b-12c)/6kJ·mol-1D.(a-3b-12c)/4kJ·mol-1
【答案】A
【解析】
依据焓变=反应物键能之和-生成物键能之和计算.
P4的结构为![]() 。则P—P键有6个,设为6x。则
。则P—P键有6个,设为6x。则
P4(g)+6Cl2(g)=4PCl3(g) ΔH=kJ·mol-1
6x 6b 12c
所以有6x +6b-12c=a
解得x=(a-6b+12c)/6
故答案为A。

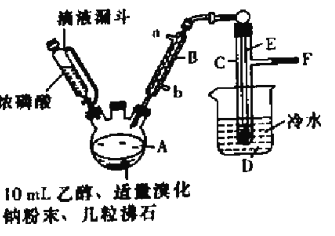
【题目】实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置),反应原理为:H3PO4(浓)+NaBr![]() +NaH2PO4+HBr,CH3CH2OH+HBr
+NaH2PO4+HBr,CH3CH2OH+HBr![]() CH3CH2Br+H2O, 有关数据见下表:
CH3CH2Br+H2O, 有关数据见下表:
物质名称 | 乙醇 | 溴乙烷 | 溴 |
状态 | 无色液体 | 无色液体 | 深红棕色液体 |
密度/gcm-3 | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
(1)A中加入沸石的作用是______________________.
(2)仪器B的名称为____________,该仪器的进水口为_______(填“a”或“b”)口.
(3)实验中用滴液漏斗代替分液漏斗的优点为_________________
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?_________(用化学方程式表示).
(5)将C中的馏出液转入锥形瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是______(保留三位有效数字)