题目内容
【题目】乙酸甲酯的催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式如下:CH3COOCH3(l)+C6H13OH(l)![]() CH3COOC6H13(l)+CH3OH(l)
CH3COOC6H13(l)+CH3OH(l)
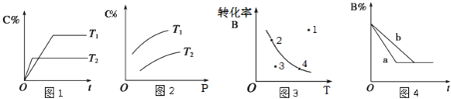
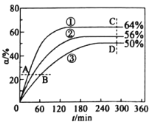
已知v正=k正×x(CH3COOCH3) ×x(C6H13OH),v逆=k逆×x(CH3COOC6H13) ×x(CH3OH),其中是k正、k逆为速率常数(受温度影响),x为各组分的物质的量分数。反应开始时,CH3COOCH3和C6H13OH按物质的量之比1:1投料,测得338K、343K、348K三个温度下CH3COOCH3转化率(![]() )随时间(
)随时间(![]() )的变化关系如图所示。下列说法正确的是
)的变化关系如图所示。下列说法正确的是
A.该反应的△H>0
B.348K时,该反应的平衡常数为1.8
C.A、B、C、D四点中,v正最大的是D
D.在曲线①、②、③中,k正与k逆的差值最大的曲线是①
【答案】AD
【解析】
A. 温度升高,反应速率加快,先达到平衡,根据图示可知①对应的温度是348K,温度升高,CH3COOCH3转化率增大,说明平衡正向移动,因此正反应为吸热反应,该反应的△H>0,A正确;
B. 反应开始时,CH3COOCH3和C6H13OH按物质的量之比1:1投料,348K时CH3COOCH3的转化率为64%,假设反应物的物质的量都是1 mol,反应前后物质的总物质的量不变,则平衡时,n(CH3COOC6H13)=n(CH3OH)=0.64 mol,n(CH3COOCH3)=n(C6H13OH)=0.36 mol,n(总)=2 mol,则该反应的平衡常数K=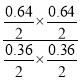 ≈3.2,B错误;
≈3.2,B错误;
C. 温度越高,物质的浓度越大,反应速率越快。根据v正=k正×x(CH3COOCH3) ×x(C6H13OH),v逆=k逆×x(CH3COOC6H13) ×x(CH3OH),A点x(CH3COOCH3) ×x(C6H13OH),温度高,因此A点v正最大,C错误;
D. k正、k逆是温度的函数,根据平衡移动的规律,k正受温度影响更大,因此温度升高,k正增大的程度大于k逆,因此,k正与k逆的差值最大的曲线是①,D正确;
故合理选项是AD。

 走进文言文系列答案
走进文言文系列答案