题目内容
【题目】

(1)该硫酸的物质的量浓度是________mol/L。
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要490 mL 4.6 mol/L的稀硫酸,则需要取________mL的该硫酸。
(3)配制时,所需的玻璃仪器除量筒、烧杯、玻璃棒和胶头滴管之外,还需要 (填仪器名称);
(4)配制溶液有如下(未按顺序排列):a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,f.将溶液移至容量瓶,g.定容等操作。其中摇匀的前一步操作是 ;(填写字母)
(5)在下列配制过程示意图中,有错误的是(填写序号) 。
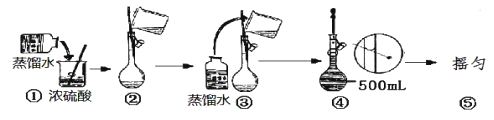
(6)在配制4.6 mol/L的稀硫酸的过程中,下列情况会引起硫酸溶液物质的量浓度偏高的是
A.未经冷却趁热将溶液注入容量瓶中 | B.容量瓶洗涤后,未经干燥处理 |
C.定容时仰视观察液面 | D.未洗涤烧杯和玻璃棒 |
【答案】(1)18.4(2)125(3)500ml容量瓶(4)g(5)14(6)A
【解析】试题分析:(1)该硫酸的物质的量浓度是![]() =18.4mol/L;(2)根据稀释前后溶质物质的量相同,
=18.4mol/L;(2)根据稀释前后溶质物质的量相同,![]() ,v=0.125L,则需要取125mL的该硫酸;(3)配制时,所需的玻璃仪器除量筒、烧杯、玻璃棒和胶头滴管之外,还需要500ml容量瓶;(4)摇匀的前一步操作是定容操作;(5)不能把水倒入浓硫酸中;定容时视线要平视刻度线;(6)未经冷却趁热将溶液注入容量瓶中,溶液体积偏小,浓度偏大;容量瓶洗涤后,未经干燥处理,无影响;定容时仰视观察液面,溶液体积偏大,浓度偏小;未洗涤烧杯和玻璃棒,溶质偏少,浓度偏小。
,v=0.125L,则需要取125mL的该硫酸;(3)配制时,所需的玻璃仪器除量筒、烧杯、玻璃棒和胶头滴管之外,还需要500ml容量瓶;(4)摇匀的前一步操作是定容操作;(5)不能把水倒入浓硫酸中;定容时视线要平视刻度线;(6)未经冷却趁热将溶液注入容量瓶中,溶液体积偏小,浓度偏大;容量瓶洗涤后,未经干燥处理,无影响;定容时仰视观察液面,溶液体积偏大,浓度偏小;未洗涤烧杯和玻璃棒,溶质偏少,浓度偏小。

练习册系列答案
相关题目