题目内容
12.已知有机物M中只含有C、H、O三种元素,其相对分子质量为88.与M有关的反应如下: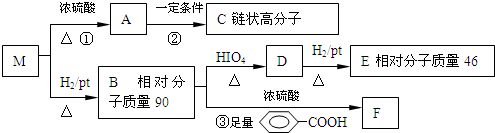
已知:
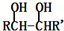 $→_{△}^{HIO_{4}}$RCHO+OHR′
$→_{△}^{HIO_{4}}$RCHO+OHR′请按要求回答下列问题:
(1)M的分子式为C4H8O2.其分子中除碳氧双键外的官能团的名称为羟基.
(2)写出①的反应类型:①消去反应.
(3)写出反应②的化学方程式:
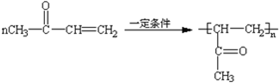 ;
;(4)X是M的同分异构体,且X属于酯类,请写出只含一个甲基的结构简式:HCOOCH2CH2CH3.
分析 根据已知反应以及D→E的反应条件可以推知D是醛,E是醇,根据E的相对分子质量为46,能求算出E为乙醇,则D为乙醛;据B→D的反应条件结合已知反应,B中应有相邻的两个-OH,B的相对分子质量为90,90-32=58,58÷12=4余10,故B的分子式应为C4H10O2,E为乙醇,则B的结构简式为CH3CHOHCHOHCH3,B与足量苯甲酸发生酯化反应,生成F,F为 ,则M为
,则M为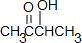 ,M→A是发生的消去反应,A为
,M→A是发生的消去反应,A为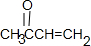 ,A→C发生加成反应,C为
,A→C发生加成反应,C为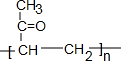 ,据此答题.
,据此答题.
解答 解:根据已知反应以及D→E的反应条件可以推知D是醛,E是醇,根据E的相对分子质量为46,能求算出E为乙醇;据B→D的反应条件结合已知反应,B中应有相邻的两个-OH,B的相对分子质量为90,90-32=58,58÷12=4余10,故B的分子式应为C4H10O2结构简式CH3CHOHCHOHCH3,E为乙醇,则B的结构简式为CH3CHOHCHOHCH3,则M为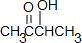 .
.
(1)则M为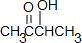 ,分子式为C4H8O2,分子中除羰基外还有羟基,
,分子式为C4H8O2,分子中除羰基外还有羟基,
故答案为:C4H8O2;羟基;
(2)M为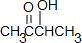 ,根据反应①的反应条件可知,①是消去反应,
,根据反应①的反应条件可知,①是消去反应,
故答案为:消去反应;
(3)M为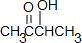 ,结合①的反应条件,M→A是发生的消去反应,羟基和右侧C上的一个H原子消去,生成一个碳碳双键,A→C是加聚反应,反应方程式为:
,结合①的反应条件,M→A是发生的消去反应,羟基和右侧C上的一个H原子消去,生成一个碳碳双键,A→C是加聚反应,反应方程式为: ,
,
故答案为: ;
;
(4)X是M的同分异构体,且X属于酯类,M的分子式为C4H8O2,只含1个甲基的只有甲酸丙酯中的HCOOCH2CH2CH3,
故答案为:HCOOCH2CH2CH3 .
点评 本题考查有机物的推断与合成,需要结合物质的相对分子质量和反应条件以及已知反应综合分析,找出突破口,难度中等.

练习册系列答案
相关题目
5.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | NaHSO3溶液:c(OH-)=c(HSO3-)+c(H+)+c(H2SO3) | |
| B. | CuSO4•(NH4)2SO4•6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>C(OH-) | |
| C. | 氯气溶于水达到平衡后,若其他条件不变加入CaCO3固体,$\frac{c({H}^{+})}{c(HClO)}$增加 | |
| D. | NaSiO3溶液加水稀释后,恢复至原温度,pH和KW均减小 |
3.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 通入过量SO2气体后的溶液:H+、Ca2+、Fe3+、N03- | |
| C. | 通入足量CO2的溶液:H+、NH4+、Al3+、SO42- | |
| D. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
17.向200mL 18mol/L H2SO4溶液中加入足量的铜片,加热使之反应,则充分反应后,被还原的H2SO4的物质的量可能是( )
| A. | 1.5mol | B. | 1.81mol | C. | 2.5mol | D. | 3.6mol |
1.下列关于离子化合物的叙述错误的是( )
| A. | 离子化合物中都含有离子键 | |
| B. | 离子化合物中可能含有共价键 | |
| C. | 在熔融状态下可以导电的化合物一定是离子化合物 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
2.下列各变化中属于原电池反应的是( )
| A. | 在空气中金属铝表面迅速氧化形成保护层 | |
| B. | 锌与稀硫酸反应时,加入少量NaHSO4固体时,可使反应速率加快 | |
| C. | 红热的铁丝与冷水接触,表面形成蓝黑色保护层 | |
| D. | 镀锌铁表面有划损时,仍然能阻止铁被氧化 |
 CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1molH2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1molH2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是 .
.