题目内容
3.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 通入过量SO2气体后的溶液:H+、Ca2+、Fe3+、N03- | |
| C. | 通入足量CO2的溶液:H+、NH4+、Al3+、SO42- | |
| D. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
分析 A.离子之间发生氧化还原反应;
B.通入过量SO2气体后的溶液,具有还原性;
C.通入足量CO2的溶液,显酸性;
D.与铝反应产生大量氢气的溶液,为非氧化性酸或强碱溶液.
解答 解:A.H+、Fe2+、NO3-发生氧化还原反应,不能大量共存,故A不选;
B.通入过量SO2气体后的溶液,具有还原性,与Fe3+(或H+、N03-)发生氧化还原反应,不能大量共存,故B不选;
C.通入足量CO2的溶液,显酸性,该组离子之间不反应,可大量共存,故C选;
D.与铝反应产生大量氢气的溶液,为非氧化性酸或强碱溶液,酸性溶液中不能大量存在CO32-,且H+、Al、NO3-发生氧化还原反应不生成氢气,故D不选;
故选C.
点评 本题考查离子的共存,为高频考点,把握题目中的信息及常见离子之间的反应即可解答,侧重氧化还原反应及复分解反应的离子共存考查,注意选项D为解答的易错点,题目难度不大.

练习册系列答案
相关题目
13.已知吡啶(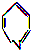 )与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
)与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
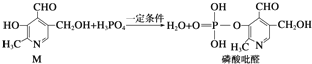
 )与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
)与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
| A. | M能使酸性高锰酸钾溶液褪色 | |
| B. | 1 mol磷酸吡醛与足量的金属钠反应,最多消耗2mol Na | |
| C. | 1 mol磷酸吡醛与NaOH溶液反应,最多消耗4mol NaOH | |
| D. | M与足量H2反应后所得有机物的分子式为C8H17O3N |
14.NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 常温常压下,8 g O2与8 g O3均含有4 NA个电子 | |
| B. | 标准状况下,2.24 L SO3的分子数为0.1 NA | |
| C. | 1L 1mol•L-1盐酸中含有NA个HCl分子 | |
| D. | 0.1 mol Fe与足量浓HNO3反应,转移电子数为0.3 NA |
18.W、X、Y、Z四种元素是原子序数依次增大的短周期主族元素,已知:①四种元素的电子层数之和等于10,且它们是连续的四种主族元素;②四种元素的原子,其半径最大的是X原子.下列说法正确的是( )
| A. | W和X均位于第二周期 | B. | Y和Z分别是Al和Si | ||
| C. | W和X分别是O和F | D. | Z的金属性可能比X强 |
8.某饱和一元醇和一元醛的混合物共3g,跟足量的银氨溶液完全反应后,可还原出16.2gAg,下列说法正确的是( )
| A. | 一定是甲醛 | B. | 可能是乙醛 | ||
| C. | 混合物中二者的质量比是1:3 | D. | 不可能有此种醛 |
9.能使酸性高锰酸钾溶液褪色而不能使溴水褪色的烃是( )
| A. | CH2=CH-CH2-CH2-CH2-CH3 | B. | HC≡C-CH2-CH2-CH2-CH3 | ||
| C. |  | D. | 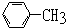 |
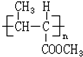 和高聚物H的合成路线如图:
和高聚物H的合成路线如图: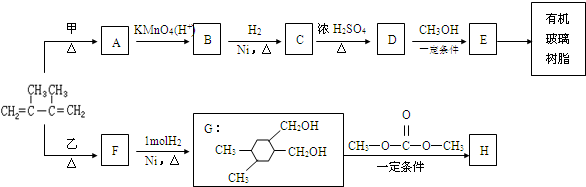
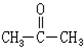 +CH3COOH
+CH3COOH
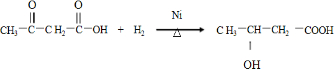 .
. .
.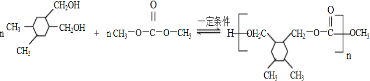 +(2n-1)CH3OH.
+(2n-1)CH3OH.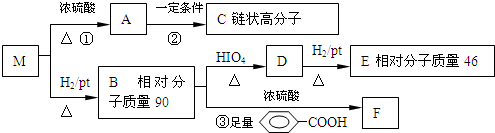
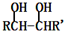 $→_{△}^{HIO_{4}}$RCHO+OHR′
$→_{△}^{HIO_{4}}$RCHO+OHR′ ;
;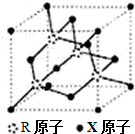 X、Y、Z、R为短周期元素,原子序数依次增大.X的基态原子的s能级电子数是p能级电子数的2倍;Y的单质在空气中含量最高;Z的氧化物是常见的两性氧化物;R基态原子最外层成对电子的数目和未成对电子的数目相等.
X、Y、Z、R为短周期元素,原子序数依次增大.X的基态原子的s能级电子数是p能级电子数的2倍;Y的单质在空气中含量最高;Z的氧化物是常见的两性氧化物;R基态原子最外层成对电子的数目和未成对电子的数目相等.