题目内容
18.如图所示装置的气密性检查中,一定漏气的是( )| A. | 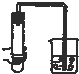 | B. |  | C. |  | D. | 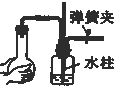 |
分析 装置气密性检验的原理是:通过气体发生器与液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏;一般用到的方法有:空气热胀冷缩法、注水法、抽气或压气法等.
解答 解:A、用手握住试管,试管内气体受热膨胀,在烧杯内有气泡产生,说明装置气密性良好,故A不选;
B、用弹簧夹夹住右边导管,向长颈漏斗中倒水,液面高度不变,说明装置气密性良好,故B不选;
C、向右拉活塞,容器内压强减小,无法证明气密性良好,故C选;
D、用弹簧夹夹住右边导管,双手捂住烧瓶,烧瓶内气体受热膨胀,使集气瓶中气体压强增大,在玻璃管中形成一段水柱,说明装置气密性良好,故D不选;故选:C.
点评 本题考查装置气密性的检查,依据的原理都是根据密闭装置中出现不同的现象来判断装置中是否存在压强差,从而判断装置是否漏气,题目难度不大.

练习册系列答案
相关题目
8.下列说法符合工业实际的是( )
| A. | 电解精炼铜时,粗铜板作阴极 | |
| B. | 冶金工业中,常用铝热反应原理冶炼钒、铬、锰等金属 | |
| C. | 工业上采取把氯气通入烧碱溶液的方法生产漂白粉 | |
| D. | 玻璃、水泥、高温结构陶瓷均为传统硅酸盐工业产品 |
6.下列有机物中,不属于烃的衍生物的是( )
| A. | 氯丁烷 | B. | 甲苯 | C. | 硝基苯 | D. | 乙酸 |
13.在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
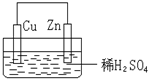

| A. | 铜片为负极 | B. | 锌片为负极 | ||
| C. | 电子通过导线由铜片流向锌片 | D. | 铜片上没有有H2逸出 |
3.下表为元素周期表的一部分,参照元素①~⑫在表中的位置,请回答下列问题.
(1)画出⑦的离子结构示意图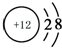 .
.
(2)⑤、⑥、⑪的原子中半径最大的是⑥(写编号).
(3)⑥和⑧的最高价的氧化物的水化物中碱性弱些的是Al(OH)3.(填化学式)
(4)④、⑩的气态氢化物中的稳定性强些的是H2O.(填化学式)
(5)写出②和⑫组成的各原子最外层电子都满足8电子的物质的化学式CCl4.
(6)写出一种由①④组成且含有非极性键的物质的电子式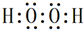 .
.
(7)③的最高价含氧酸的稀溶液与铜粉反应的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(8)利用较强酸能制出较弱酸的原理,写出一个能证明②和⑨非金属性强弱的一个常见反应的化学方程式Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
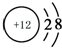 .
.(2)⑤、⑥、⑪的原子中半径最大的是⑥(写编号).
(3)⑥和⑧的最高价的氧化物的水化物中碱性弱些的是Al(OH)3.(填化学式)
(4)④、⑩的气态氢化物中的稳定性强些的是H2O.(填化学式)
(5)写出②和⑫组成的各原子最外层电子都满足8电子的物质的化学式CCl4.
(6)写出一种由①④组成且含有非极性键的物质的电子式
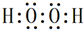 .
.(7)③的最高价含氧酸的稀溶液与铜粉反应的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(8)利用较强酸能制出较弱酸的原理,写出一个能证明②和⑨非金属性强弱的一个常见反应的化学方程式Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3.
7.迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.下列叙述正确的是( )


| A. | 1mol迷失香酸最多能和含6molNaOH的水溶液完全反应 | |
| B. | 1mol迷迭香酸最多能和9mol氢气发生加成,和6mol溴发生取代反应 | |
| C. | 迷迭香酸属于芳香烃 | |
| D. | 迷迭香酸可以发生水解、消去、取代和酯化反应 |