题目内容
(6分)在50mL a mol·L-1的硝酸溶液中,加入6.4g Cu,全部溶解,假设硝酸的还原产物只有NO2和NO,将反应后溶液用蒸馏水稀释至100mL时测得c(NO3-)="3" mol·L-1。
(1)求稀释后的溶液的pH= 。
(2)若a=9,则生成的气体中NO2的物质的量为 mol。
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
若将上述的NO2和NO的混合气体通入1mol·L-1的NaOH恰好被吸收,求NaOH溶液的体积为 mL。
(1)求稀释后的溶液的pH= 。
(2)若a=9,则生成的气体中NO2的物质的量为 mol。
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
若将上述的NO2和NO的混合气体通入1mol·L-1的NaOH恰好被吸收,求NaOH溶液的体积为 mL。
(6分)(1)0 (2)0.125 mol (3)150(各2分)
试题分析:(1)Cu的物质的量是0.1mol,反应后的溶液中NO3-的物质的量是0.3mol,说明反应后的溶液为硝酸铜与硝酸的混合液,根据电荷守恒,其中氢离子的物质的量是0.1mol,浓度是1mol/L,所以稀释后溶液的pH=0;
(2)若a=9,则原硝酸溶液中硝酸的物质的量是0.45mol,根据(1)可知反应后溶液中NO3-的物质的量是0.3mol,所以被还原的硝酸的物质的量是0.15mol,设混合气体中NO2的物质的量为xmol,NO的物质的量是ymol,则x+y=0.15,x+3y=0.1×2,解得x=0.125mol,y=0.025mol;
(3)根据(2)的结果,结合化学方程式计算需要氢氧化钠的物质的量是0.15mol,所以1mol·L-1的NaOH溶液的体积是150mL。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
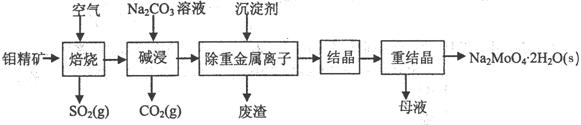 (1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________
(1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________
 Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。
Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。

