题目内容
18.某烃结构简式如图: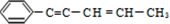 ,有关其结构说法正确的是( )
,有关其结构说法正确的是( )| A. | 所有原子可能在同一平面上 | B. | 所有原子不可能在同一条直线上 | ||
| C. | 所有碳原子可能在同一平面上 | D. | 该烃属于苯的同系物 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断.
解答 解:有机物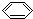 -C≡C-CH=CH-CH3中,具有苯环、乙烯的共面结构以及乙炔的共线结构,所以苯环的6个碳原子一定共面,具有乙烯结构的后4个碳原子一定共面,具有乙炔结构的两个碳原子(倒数第四个和倒数第五个)一定共线,所有的碳原子可以共面,但不共线;该有机物含有甲基,为四面体结构,所有原子不可能在同一条直线上;该烃含有碳碳双键、碳碳三键,不属于苯的同系物;
-C≡C-CH=CH-CH3中,具有苯环、乙烯的共面结构以及乙炔的共线结构,所以苯环的6个碳原子一定共面,具有乙烯结构的后4个碳原子一定共面,具有乙炔结构的两个碳原子(倒数第四个和倒数第五个)一定共线,所有的碳原子可以共面,但不共线;该有机物含有甲基,为四面体结构,所有原子不可能在同一条直线上;该烃含有碳碳双键、碳碳三键,不属于苯的同系物;
故选BC.
点评 本题考查学生有机物的基本结构知识,属于基本知识题目,难度不大,可以根据所学知识来回答.

练习册系列答案
相关题目
8.以下说法错误的是( )
| A. | 银氨溶液可用于区分麦芽糖和葡萄糖 | |
| B. | 乙烷、乙醛、乙酸的沸点逐渐升高 | |
| C. | 1mol乙酰水杨酸(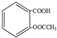 )最多可以和3molNaOH反应 )最多可以和3molNaOH反应 | |
| D. | 邻甲基苯酚(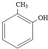 )可以和HCHO发生缩聚反应 )可以和HCHO发生缩聚反应 |
9.下列化学用语表达正确的是( )
| A. | 一氯乙烷的结构式CH3Cl | B. | 丁烷的结构简式CH3CH2CH2CH3 | ||
| C. | 四氯化碳的电子式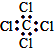 | D. | 乙烷的分子式 (CH3)2 |
6.如图,在锌、铜和硫酸组成的原电池中,负极发生的反应是( )
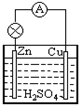

| A. | Zn-2e-=Zn2+ | B. | Cu-2e-=Cu2+ | C. | 2H++2e-=H2↑ | D. | Cu2++2e-=Cu |
13.根据总反应式:Zn+Cu2+=Zn2++Cu,请分析下述原电池的组成,对应正确的一组是( )
| A | B | C | D | |
| 正极 | Cu | Cu | Zn | Ag |
| 负极 | Zn | Zn | Cu | Cu |
| 电解质溶液 | CuSO4 | AgNO3 | CuCl2 | CuSO4 |
| A. | A | B. | B | C. | C | D. | D |
3.下表是元素周期表的一部分,表中的每个字母代表一种短周期元素.
(1)a元素和c元素可以形成的气体,其化学式为NH3;
(2)e的元素符号是Na;
(3)b元素原子的最外层电子数为4;
(4)b、c、d三种元素的非金属性逐渐增强(填“减弱”或“增强”);
(5)d元素和f元素均可形成气态氢化物,其稳定性为H2d大于H2f (填“大于”或“小于”).
(6)上述七种元素的最高价氧化物的水合物中,碱性最强的是NaOH,酸性最强的是HClO4,既有酸性又有碱性的是Al(OH)3(写化学式)
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | d | |||||
| 3 | e | g | f | |||||
(2)e的元素符号是Na;
(3)b元素原子的最外层电子数为4;
(4)b、c、d三种元素的非金属性逐渐增强(填“减弱”或“增强”);
(5)d元素和f元素均可形成气态氢化物,其稳定性为H2d大于H2f (填“大于”或“小于”).
(6)上述七种元素的最高价氧化物的水合物中,碱性最强的是NaOH,酸性最强的是HClO4,既有酸性又有碱性的是Al(OH)3(写化学式)
10.常温下,0.1mol•L-1HX的pH=1,0.1mol•L-1CH3COOH的pH=2.9.下列说法不正确的是( )
| A. | HX和CH3COOH均可抑制水的电离 | |
| B. | 将HX与CH3COOH 各0.1mol溶于水配成1L混合溶液,则溶液的c(H+)=0.2 mol•L-1 | |
| C. | 将等物质的量浓度、等体积的HX与CH3COONa两溶液混合后所得溶液中:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+) | |
| D. | 0.3mol•L-1的CH3COOK溶液:c(CH3COO-)+c(CH3COOH)=c(K+) |
7.下列物质的分子中,所有的原子都在同一平面上的是( )
| A. | 甲烷 | B. | 乙烯 | C. | 甲苯 | D. | 溴乙烷 |
8.有A、B、C、D四种金属.将A与B用导线连接起来浸入稀硫酸中,B上有气泡产生;将A、D分别投入到等浓度的稀盐酸中,D比A反应剧烈;将Cu浸入B的盐溶液中,无明显变化;如果把Cu浸入C的盐溶液中,有金属C析出.据此判断它们的活动性由强到弱顺序是( )
| A. | C>B>A>D | B. | D>A>B>C | C. | D>B>A>C | D. | B>A>D>C |