题目内容
6.如图,在锌、铜和硫酸组成的原电池中,负极发生的反应是( )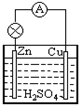
| A. | Zn-2e-=Zn2+ | B. | Cu-2e-=Cu2+ | C. | 2H++2e-=H2↑ | D. | Cu2++2e-=Cu |
分析 锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应;铜作正极,正极上氢离子得电子发生还原反应,据此回答判断.
解答 解:锌作负极,负极上锌失电子发生氧化反应,Zn-2e-═Zn2+,故选A.
点评 本题考查原电池原理,明确正负极上得失电子是解本题关键,难度不大,注意对基础知识的归纳整理.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
16.下列表示的是有机化合物结构式中的一部分,其中不是官能团的是( )
| A. | -OH | B. | -C≡C- | C. |  | D. | C-C |
17.法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”.下列有关“四中子”粒子的说法不正确的是( )
| A. | 该粒子不显电性 | B. | 该粒子质量数为4 | ||
| C. | 与氢元素的质子数相同 | D. | 该粒子质量比氢原子大 |
14.如图图元素周期表的一部分,下列说法中正确的是( )
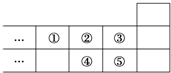

| A. | 元素①位于第2周期第ⅣA族 | |
| B. | ①的气态氢化物与⑤的气态氢化物反应产生白烟 | |
| C. | 元素的氧化物对应水化物的酸性一定是:⑤>④ | |
| D. | 元素的最高正化合价:③=⑤ |
1.下列各组离子在给定条件下能大量共存的是( )
| A. | 强酸性溶液中:NH4+、K+、CO32-、Cl- | |
| B. | 有SO42-存在的溶液中:Na+、Mg2+、Ba2+、I- | |
| C. | 加入铝粉能放出氢气的溶液中:K+、Ba2+、Cl-、Br- | |
| D. | 在强碱性的溶液中:NH4+、Na+、Cl-、H+ |
11.下列化学用语书写正确的是( )
| A. | 氯离子的结构示意图: | |
| B. | CCl4的电子式: | |
| C. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| D. | 用电子式表示氯化氢分子的形成过程:H+ → → |
18.某烃结构简式如图: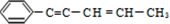 ,有关其结构说法正确的是( )
,有关其结构说法正确的是( )
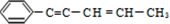 ,有关其结构说法正确的是( )
,有关其结构说法正确的是( )| A. | 所有原子可能在同一平面上 | B. | 所有原子不可能在同一条直线上 | ||
| C. | 所有碳原子可能在同一平面上 | D. | 该烃属于苯的同系物 |
16.如图是某有机物分子的简易球棍模型.下列关于该有机物的说法中错误的是( )


| A. | 分子式为C3H7O2N | |
| B. | 该有机物能发生缩聚反应 | |
| C. | 能通过聚合反应生成高分子化合物 | |
| D. | 具有相同官能团的该有机物的同分异构体还有两种 |
 ,
, .两种离子中,半径较小的是Na+(填离子符号).
.两种离子中,半径较小的是Na+(填离子符号). B2C2
B2C2 .
.