题目内容
【题目】已知25 ℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8×10-5 |
| Ka=3.0×10-8 |
(1)物质的量浓度均为0.1 mol·L-1的下列四种溶液,pH由小到大排列的顺序是__________(用编号填写)。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1 mol·L-1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是__________(填字母)。
a. ![]() b.
b. ![]() c.
c. ![]()
d. ![]() e.
e. ![]()
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式__________。
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中:c(CH3COO-)-c(Na+)=__________(填准确数值)。
(5)25℃时,将a mol·L-1的醋酸与b mol·L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离常数为__________
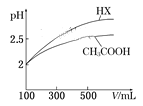
(6)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数__________(填“>”、”=”或“<”)CH3COOH的电离平衡常数。
【答案】a<d<c<b bd ClO-+CO2+H2O=HCO3-+HClO 9.9×10-7 mol·L-1(或10-6-10-8) 107×b/(ab) >
【解析】
(1)弱酸的电离平衡常数越大,其酸性越强,其酸根的水解程度越弱;
(2)0.1mol/L的CH3COOH溶液加水稀释过程中,氢离子与醋酸根离子物质的量增大,醋酸分子物质的量减小,浓度减小,酸性减弱,水的离子积常数不变,醋酸的电离平衡常数不变;
(3)向次氯酸钠溶液中通入少量二氧化碳的离子方程式为ClO-+CO2+H2O=HCO3-+HClO;
(4)根据溶液中的电荷守恒和物料守恒来计算;
(5)根据电离常数的公式进行计算;
(6)据图分析,加水稀释的过程中,HX的pH变化比较快,说明HX的酸性比醋酸强,电离程度:HX>CH3COOH。
(1)据电离平衡常数可知,酸性由强到弱的顺序为:CH3COOH>H2CO3>HClO>HCO3-,弱酸的酸性越弱其酸根离子的水解程度越大,溶液碱性越强,所以pH由小到大排列顺序是a<d<c<b,故答案为:a<d<c<b。
(2)a.0.1molL﹣1的CH3COOH溶液加稀释过程中,电离程度增大,氢离子浓度减小,故a错误;
b.0.1molL﹣1的CH3COOH溶液加稀释过程中,微粒浓度减小,同时醋酸的电离向右移动,c(H+)减小的程度小于c(CH3COOH)的减小程度,所以c(H+)/c(CH3COOH)增大,故b正确;
c.Kw=c(H+)c(OH﹣)只受温度的影响,温度不变则其值是一个常数,故c错误;
d.醋酸稀释,酸性减弱,c(H+)减小,碱性增强,c(OH﹣)增大,即c(OH﹣)/c(H+)增大,故d正确;
e.该比值表示电离平衡常数,温度不变,平衡常数不变,故e错误。
故答案为:bd。
(3)向次氯酸钠溶液中通入少量二氧化碳的离子方程式为ClO-+CO2+H2O=HCO3-+HClO,故答案为:ClO-+CO2+H2O=HCO3-+HClO。
(4)CH3COOH与CH3COONa的混合溶液中,存在电荷守恒:c(Na+)+c(H+)=c(OH﹣)+c(CH3COO﹣),所以c(CH3COO﹣)﹣c(Na+)=c(H+)﹣c(OH﹣)=10﹣6mol/L﹣10﹣8mol/L=9.9×10﹣7mol/L,故答案为:9.9×10-7 mol·L-1(或10-6-10-8)。
(5)将amolL-1的醋酸溶液与bmolL-1的氢氧化钠溶液等体积混合,溶液呈中性,说明醋酸过量,醋酸和氢氧化钠溶液发生反应CH3COOH+NaOH=CH3COONa+H2O,则溶液中c(CH3COOH)=(ab)/2molL-1,达到电离平衡时,溶液呈中性,氢离子浓度是1×10-7molL-1,c(Na+)=c(CH3COO-)=b/2molL-1,则k=c(CH3COO)×c(H+)/c(CH3COOH)=107×b/(ab),故答案为:107×b/(ab)。
(6)根据CH3COOH与一元酸HX加水稀释过程中pH与溶液体积的关系图可以看出HX酸在稀释过程中溶液的pH变化比醋酸的大,所以酸性HX强于醋酸,电离程度:HX>CH3COOH,故答案为:>。

【题目】实验室以苯甲醛为原料制备间溴苯甲醛的反应如下:
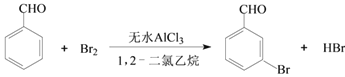
已知:(1)间溴苯甲醛温度过高时易被氧化。
(2)溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的沸点及相对分子质量见下表:
物质 | 溴 | 苯甲醛 | 1,2-二氯乙烷 | 间溴苯甲醛 |
沸点/℃ | 58.8 | 179 | 83.5 | 229 |
相对分子质量 | 160 | 106 | 185 |
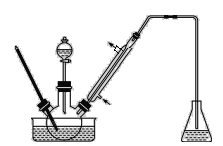
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后装入三颈烧瓶(如图所示),缓慢滴加经浓硫酸干燥过的足量液溴,控温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤出MgSO4nH2O晶体。
步骤4:减压蒸馏有机层,收集相应馏分。
(1)实验装置中冷凝管的主要作用是_________,锥形瓶中应为_____(填化学式)溶液。
(2)步骤1反应过程中,为提高原料利用率,适宜的温度范围为(填序号)_______。
A.>229℃ B.58.8℃~179℃ C.<58.8℃
(3)步骤2中用10% NaHCO3溶液洗涤,是为了除去溶于有机层的_______(填化学式)。
(4)步骤3中加入无水MgSO4固体的作用是_____________。
(5)步骤4中采用减压蒸馏,是为了防止__________________________________。
(6)若实验中加入了5.3 g苯甲醛,得到3.7 g间溴苯甲醛。则间溴苯甲醛产率为______。