题目内容
3.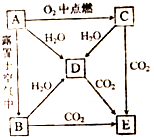 A、B、C、D、E五中物质中都含有钠元素,其互相转化关系如题:
A、B、C、D、E五中物质中都含有钠元素,其互相转化关系如题:(1)写出B的电子式
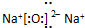 .
.(2)写出A→D的离子方程式2Na+2H2O=2Na++2OH-+H2↑.
(3)写出C→E的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
分析 A在氧气中燃烧生成C,A在空气中短期接触生成B,A与水反应生成D,且A、B、C都能和水反应生成D,A、C都是氧化物,都和水反应生成D,D只能为碱,A的元素为短周期元素,故A为Na,C为Na2O2,D为NaOH,E是Na2CO3,Na在空气中短期接触生成B,B为Na2O,Na2O与CO2反应生成Na2CO3,与水反应生成NaOH,符合转化关系,据此解答.
解答 解:A在氧气中燃烧生成C,A在空气中短期接触生成B,A与水反应生成D,且A、B、C都能和水反应生成D,A、C都是氧化物,都和水反应生成D,D只能为碱,A的元素为短周期元素,故A为Na,C为Na2O2,D为NaOH,E是Na2CO3,Na在空气中短期接触生成B,B为Na2O,Na2O与CO2反应生成Na2CO3,与水反应生成NaOH,符合转化关系,
(1)B为Na2O,B的电子式为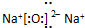 ,
,
故答案为: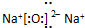 ;
;
(2)A→D的反应为钠与水的反应,其离子方程式为2Na+2H2O=2Na++2OH-+H2↑,故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(3)C→E是二氧化碳与过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2.
点评 本题考查无机物推断,涉及Na元素单质及其化合物之间的相互转化关系,难度中等,结合转化关系判断D为碱是关键,推断金属A为Na,然后进行验证.

练习册系列答案
相关题目
13.配制一定体积,一定物质的量浓度溶液时,下列情况中溶液的浓度偏小的是( )
| A. | 溶解后,溶液未经冷却,立即转移至容量瓶 | |
| B. | 胶头滴管滴加蒸馏水时,不小心把少量的蒸馏水滴到容量瓶外 | |
| C. | 转移溶液后,未洗涤烧杯和玻璃棒就直接定容 | |
| D. | 定容时,俯视刻度线 |
14.下列变化中,属于吸热反应的是( )
| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | ||
| C. | 铝粉与氧化铁粉末反应 | D. | 氧化钙溶于水 |
11.已知在密闭容器中发生的反应:H2(g)+I2(g)?2HI(g)△H<0.若改变下列条件,则其反应速率发生的变化是(在表格的相应空格内填“√”)
| 序号 | 改变条件 | 反应速率变化 | ||
| 增大 | 减小 | 不变 | ||
| (1) | 升高温度 | |||
| (2) | 充入更多的H2 | |||
| (3) | 扩大容器的体积 | |||
| (4) | 定容充入氦气 | |||
18.青奥会于2014年8月在南京圆满举行,青奥会建筑设施使用了大量节能材料,体现了“绿色青奥”的理念,下列说法正确的是( )
| A. | 用于青奥村工程隔热保温材料聚氨酯属于有机高分子材料 | |
| B. | 青奥会议中心双塔采用了玻璃幕墙设计,制造玻璃的主要原料为纯碱和石灰石 | |
| C. | 青奥中心外墙的复合保温材料采用铝合金锁边,铝合金比金属铝更具有强度大、耐腐蚀的优点 | |
| D. | 青奥会健身中心的地面采用了聚苯乙烯保温板,聚苯乙烯的结构简式为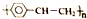 |
8.如图所示,a、b两电极材料分别为铁丝和铜丝.则以下说法不正确的是( )
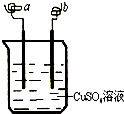

| A. | 该装置可以构成原电池,也可构成电解池 | |
| B. | a 极可能发生反应:Cu2++2e-→Cu | |
| C. | b 电极质量可能增加 | |
| D. | 该过程可能有大量气体产生 |
15.下列说法正确的是( )
| A. | “钡餐”中使用的硫酸钡是弱电解质 | |
| B. | 太阳能电池板中的硅在周期表中处于金属与非金属的交界位置 | |
| C. | 常用的自来水消毒剂有Cl2和二氧化氯,两者都含极性键 | |
| D. | “滴水穿石”不涉及化学变化 |
12.已知某混合金属粉末,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上.请设计合理实验探究该混合物金属粉末中铁、铜元素的存在.仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液.
完成以下实验探究过程:
(1)提出假设:
假设1 该混合金属粉末中除铝外还含有Fe(或Cu)元素;
假设2 该混合金属粉末中除铝外还含有Cu(或Fe)元素;
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案(不要在答题卡上作答).
(3)实验过程
根据(2)的实验方案,完成实验操作、预期现象和结论的有关问题.
完成以下实验探究过程:
(1)提出假设:
假设1 该混合金属粉末中除铝外还含有Fe(或Cu)元素;
假设2 该混合金属粉末中除铝外还含有Cu(或Fe)元素;
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案(不要在答题卡上作答).
(3)实验过程
根据(2)的实验方案,完成实验操作、预期现象和结论的有关问题.
| 编号 | 实验操作 | 预期现象 | 结论 |
| ① | 用药匙取少许样品,加入试管A中,再用滴管取过量NaOH溶液并滴加到试管A中,充分反应后,静置,弃去上层清液,剩余固体备用 | 样品部分溶解,并有气体放出 | |
| ② | 往试管A的剩余固体中加过量稀硫酸,充分反应后,静置.取上层清液于试管B中,剩余固体备用 | 固体部分溶解,并有气体放出,溶液呈浅绿色 | 可能含铁 (填元素名称,以下同) |
| ③ | 往试管B中加入少许稀硝酸,再滴加KSCN溶液 | 溶液先变黄色,加KSCN后显血红色 | 结合②可知,一定含 |
| ④ | 往②剩余固体中加入稀硝酸,再滴加NaOH溶液 | 固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色,加NaOH溶液后有蓝色 沉淀产生. | 一定含铜. |
13.下列各项中表达正确的是( )
| A. | 氟原子的结构示意图: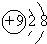 | B. | 乙烯结构式:CH2=CH2 | ||
| C. | 乙炔球棍模型: | D. | NH3的电子式: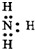 |