题目内容
4.下列物质 ①CO2 ②NH3 ③氢氧化钠溶液 ④H2SO4 ⑤乙醇⑥Fe(OH)3胶体 ⑦NaHCO3其中属于属于酸的是④;其中属于混合物的是③⑥;其中属于电解质的是④⑦;其中属于盐的是⑦.( 填序号)
分析 混合物由两种或两种以上不同物质组成的物质;
酸是指在电离时产生的阳离子全部是氢离子的化合物;
电解质是在熔融状态或水溶液中能导电的化合物;
盐是指在电离时生成金属离子或铵根离子(NH4+)与酸根离子或非金属离子的化合物.
解答 解:④H2SO4电离时产生的阳离子全部是氢离子,属于酸;
③氢氧化钠溶液 ⑥Fe(OH)3胶体是由多种物质组成的,属于混合物;
④H2SO4 ⑦NaHCO3在熔融状态下或水溶液中能导电,属于电解质;
⑦NaHCO3电离时产生钠离子和碳酸氢根离子,属于盐;
故答案为:④;③⑥;④⑦;⑦.
点评 本题考查混合物、电解质、酸等概念,题目难度不大,但涉及物质较多,注意不要漏选.

练习册系列答案
相关题目
14.试回答下列各题:
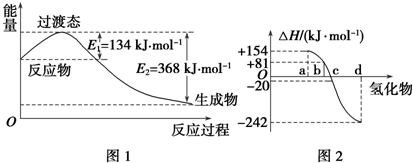
(1)如图1所示是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234 kJ•mol-1.
(2)化学反应的焓变与反应物和生成物的键能有关.
①已知:H2(g)+Cl2(g)═2HCl(g)△H=-185kJ•mol-1
请填空:
②图2中表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢在热力学标准状态下,发生分解反应的热化学方程式:H2Se(g)═Se(s)+H2(g)△H=-81 kJ•mol-1.
(3)已知:Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-25kJ•mol-1①
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47kJ•mol-1②
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+19kJ•mol-1③
请写出CO还原FeO的热化学方程式:CO(g)+FeO(s)═Fe(s)+CO2(g)△H=-11 kJ•mol-1.

(1)如图1所示是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234 kJ•mol-1.
(2)化学反应的焓变与反应物和生成物的键能有关.
①已知:H2(g)+Cl2(g)═2HCl(g)△H=-185kJ•mol-1
请填空:
| 共价键 | H-H | Cl-Cl | H-Cl |
| 键能/(kJ•mol-1) | 436 | 247 | 434 |
(3)已知:Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-25kJ•mol-1①
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47kJ•mol-1②
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+19kJ•mol-1③
请写出CO还原FeO的热化学方程式:CO(g)+FeO(s)═Fe(s)+CO2(g)△H=-11 kJ•mol-1.
16.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,22.4 L CCl4中所含分子数为NA | |
| B. | 标准状况下,18g水所含原子数为NA | |
| C. | 常温常压下,11.2 LCO2所含的原子数为1.5NA | |
| D. | 常温常压下,48 g O2与O3混合物含有的氧原子数为3NA |
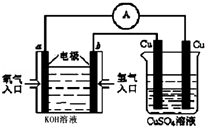 氨气是一种重要工业原料,在工农业生产中具有重要的应用.
氨气是一种重要工业原料,在工农业生产中具有重要的应用.