题目内容
9.实验室需要配制0.100mol•L-1的Na2CO3溶液490mL.可供选用的仪器有:①胶头滴管 ②量筒 ③烧杯 ④玻璃棒 ⑤托盘天平(包括砝码盒)请回答下列问题:(1)配制上述溶液时,需要Na2CO3固体的质量为5.3 g.
(2)除上述仪器外,完成该实验还缺少的仪器有药匙、500 mL容量瓶(写仪器名称).
(3)配制过程中的下列操作,对所配溶液的浓度有何影响?(用“偏高”、“偏低”和“无影响”填空)
①如果烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外:偏低;
②如果定容时俯视刻度:偏高;
③如果定容摇匀后,发现液面低于刻度线,加水至液面与刻度线相切偏低.
分析 (1)配制490mL0.100mol•L-1的Na2CO3溶液,实验室没有490mL容量瓶,应选择500mL容量瓶,依据m=CVM计算需要溶质的质量;
(2)依据配制一定物质的量浓度溶液的一般步骤确定使用的仪器;
(3)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)配制490mL0.100mol•L-1的Na2CO3溶液,实验室没有490mL容量瓶,应选择500mL容量瓶,需要碳酸钠的质量m=0.1mol/L×0.5L×106g/mol=5.3g;
故答案为:5.3;
(2)配制一定物质的量浓度溶液一般步骤为:计算、称量取、溶解、冷却、移液、洗涤、定容、摇匀等,
用到的仪器有:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以还缺少的是:药匙、500 mL容量瓶;
故答案为:药匙、500 mL容量瓶;
(3)①如果烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,导致溶质的物质的量偏小,溶液浓度偏低;
故答案为:偏低;
②如果定容时俯视刻度,导致溶液体积偏小,溶液浓度偏高;
故答案为:偏高;
③如果定容摇匀后,发现液面低于刻度线,加水至液面与刻度线相切,导致溶液体积偏大,溶液浓度偏低;
故答案为:偏低.
点评 本题考查了配制一定物质的量浓度溶液,明确配制原理及操作步骤是解题关键,注意容量瓶规格的选择和误差分析的方法,题目难度不大.

练习册系列答案
相关题目
20.下列说法正确的是( )
| A. | 一定条件下,增大反应物的量会加快化学反应速率 | |
| B. | 能够发生有效碰撞的分子叫活化分子 | |
| C. | 活化分子间所发生的碰撞为有效碰撞 | |
| D. | 增大压强,肯定会加快化学反应速率 |
17.K、L、Z、W、R属于短周期主族元素.K的原子半径是短周期主族元素中最大的,L元素的单质常通过分离液态空气得到,Z元素的单质是常见的半导体材料,W与Z同族,R与L同族,其单质有杀菌作用. 下列叙述不正确的是( )
| A. | K与L形成的两种化合物中阴、阳离子的个数比均为1:2,且均能与水反应 | |
| B. | 根据非金属性强弱,不可能由Z的最高价氧化物制出W的最高价氧化物 | |
| C. | L的简单氢化物的沸点和热稳定性均大于R的简单氢化物 | |
| D. | 向两份BaCl2溶液中分别通入RL2、WL2,均无白色沉淀生成,但一段时间后,通入RL2的一份中可能产生沉淀 |
1.下列表述正确的是( )
| A. | .氢氧根离子的电子式是: | |
| B. | •二氧化碳分子的比例模型是 | |
| C. | .芳香烃的组成通式是CnH2n-6(n≥6) | |
| D. | .12C和14C的原子结构示意图均可表示为  |
18.下列有关钠的化合物的叙述不正确的是( )
| A. | Na2O2可用作呼吸面具供氧剂,它还可以用于消毒、杀菌和漂白 | |
| B. | NaH可用于和水反应制取氢气,NaH是共价化合物 | |
| C. | Na2CO3的水溶液可用于油污的去除,其热溶液去污效果更好 | |
| D. | 侯氏制碱法,首先制取的是NaHCO3,NaHCO3受热分解生成碳酸钠 |
19.能正确表示下列化学反应的离子方程式的是( )
| A. | CuO溶解在稀盐酸中:O2-+2H+═H2O | |
| B. | 硫酸溶液中滴加氢氧化钡溶液:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | 金属钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
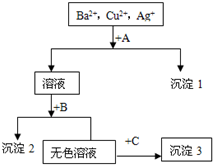
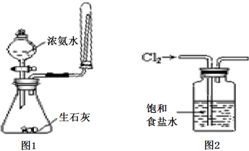 以下说法正确的是( )
以下说法正确的是( )