题目内容
11.2014年5月7日,天津某公司在南京丢失一枚放射源:铱-192( ${\;}_{77}^{192}$Ir),环保部定性为重大辐射事故.下列有关${\;}_{77}^{192}$Ir的说法中正确的是( )| A. | ${\;}_{77}^{192}$Ir原子核内含有192个质子 | |
| B. | ${\;}_{77}^{192}$Ir 和${\;}_{77}^{191}$Ir互为同位素 | |
| C. | ${\;}_{77}^{192}$Ir原子核内含有77个中子 | |
| D. | ${\;}_{77}^{192}$Ir的电子数为115 |
分析 具有相同质子数,不同中子数的同一元素的不同核素互为同位素同位素,元素符号的左上角数字代表质量数A,左下角数字代表质子数Z,中子数N=质量数A-质子数Z.
解答 解:A.77192I 原子核内含有77个质子,故A错误;
B、${\;}_{77}^{192}$Ir 和${\;}_{77}^{191}$Ir具有有相同质子数,不同中子数,互为同位素,故B正确;
C.77192I 原子核内含有192-77=115个中子,故C错误;
D.77192I 原子的核外电子数总数为77,故D错误.
故选B.
点评 本题考查同位素的概念,难度不大,注意同位素概念的掌握以及原子中质子数、质量数的辨析.

练习册系列答案
相关题目
5.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A. | 常温下,CH3COONa和CH3COOH混合溶液中[pH=7,c(Na+)=0.1mol•L-1]:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | |
| B. | 在O.1mol•L-1Na2C03溶液中:cc(Na+)=2c(CO32-) | |
| C. | 在O.1mol•L-1NaHC03溶液中:c(HCO3-)>c(CO32-)>c(H2C03) | |
| D. | 向0.2mol•L-1NaHC03溶液中加入等体积O.1mol•L-1NaOH溶液:c(CO32-)+c(HCO3-)+c(OH-)=c(H+)+c(Na+) |
16.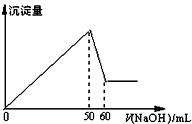 在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度
在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度
之比为( )
 在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度
在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度之比为( )
| A. | 1:1 | B. | 3:1 | C. | 1:2 | D. | 2:1 |
20.原电池的构造如图所示,下列说法不正确的是( )
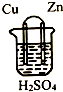

| A. | 铜片作正极,锌片作负极 | |
| B. | 该电池工作时,锌失电子变为Zn2+进入溶液 | |
| C. | 该电池工作时,电子由铜片流向锌片 | |
| D. | 该电池工作时,H+在铜片上得电子被还原生成H2逸出 |
1.下列水解反应的应用,不正确的是( )
| A. | CO32-+H2O?HCO3-+OH- 热的纯碱溶液清洗油污 | |
| B. | Al3++3H2O?Al(OH)3 (胶体)+3 H+ 明矾净水 | |
| C. | TiCl4+(x+2)H2O(过量)?TiO2•x H2O+4HCl 用TiCl4制备TiO2 | |
| D. | SnCl2+H2O?Sn(OH)Cl+HCl 配制氯化亚锡溶液时应加入氢氧化钠 |
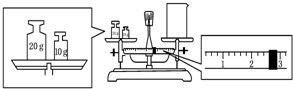 实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液250mL:
实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液250mL: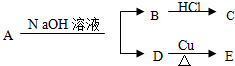 ,又已知D不与Na2CO3溶液反应,C和E都不能发生银镜反应.A的结构可能有( )
,又已知D不与Na2CO3溶液反应,C和E都不能发生银镜反应.A的结构可能有( )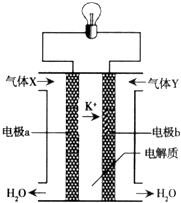 氢氧燃料电池已用于航天飞机.以30% KOH溶液为电解质溶液的这种电池的构造如图所示.该电池在工作时的电极反应如下:
氢氧燃料电池已用于航天飞机.以30% KOH溶液为电解质溶液的这种电池的构造如图所示.该电池在工作时的电极反应如下: