题目内容
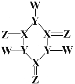
【题目】某化合物的结构如图所示,分子中所有原子都达到了 8电子稳定结构,X、Y、Z、W是原子序数依次增大的短周期主族元素,原子半径:r(X)>r(Y)>r(Z),W的单质可用来制取漂白剂和自来水消毒。下列说法正确的是
A.YZ2属于酸性氧化物
B.X的氧化物的水化物酸性弱于W的氧化物的水化物酸性
C.X、Y、Z与氢元素均可形成含非极性键的二元化合物
D.Z分别与W、X、Y形成的二元化合物均不止一种
【答案】CD
【解析】
化合物分子中所有原子都达到了8电子稳定结构。X、Y、Z、W是原子序数依次增大的短周期主族元素,W的单质可用来制取漂白剂和自来水消毒,则W是Cl元素;原子半径r(X)>r(Y)>r(Z),同一周期原子序数越大原子半径越小,Z能够形成1个双键,X形成4个共价键,Y形成3个共价键,W形成1个共价键,W位于第三周期,X、Y、Z位于第二周期,X为C,Y为N,Z为O,W为Cl元素,据此解答。
根据分析可知,X为C,Y为N,Z为O,W为Cl元素。
A. YZ2是NO2,NO2与NaOH溶液反应产生NaNO3、NaNO2、H2O,反应中N元素化合价发生了变化,因此NO2不属于酸性氧化物,A错误;
B. X形成的氧化物有CO、CO2,CO难溶于水,CO2溶于水反应产生的H2CO3为弱酸,而Cl元素的氧化物对应的酸有多种,如HClO是一元弱酸,酸性比碳酸弱,而HClO3、HClO4都是强酸,可见未指明氧化物的价态,无法比较相应的物质的酸性强弱,B错误;
C. C与H形成CH3-CH3、CH2=CH2等、N与H可形成NH2-NH2及O与H可形成H2O2中含有非极性键;故C、N、O三种元素均可以与氢元素均可形成含非极性键的二元化合物,C正确;
D. Cl元素的氧化物有Cl2O、Cl2O3、ClO2、Cl2O5等,C元素的氧化物有CO、CO2等,N元素的氧化物有NO、NO2、N2O3、N2O4等,因此Z分别与W、X、Y形成的二元化合物均不止一种,D正确;
故合理选项是CD。

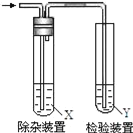
【题目】欲要检验不同条件下制得的乙烯,四个实验小组均用图所示装置对所制得的进行除杂、检验,所用试剂X、Y分别见下表所示.你认为设计中不需要除杂的小组是( )
小组 | 乙烯的制备 | 试剂X | 试剂Y |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
C | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | Br2的CCl4 |
A.AB.BC.CD.D