题目内容
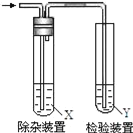
【题目】欲要检验不同条件下制得的乙烯,四个实验小组均用图所示装置对所制得的进行除杂、检验,所用试剂X、Y分别见下表所示.你认为设计中不需要除杂的小组是( )
小组 | 乙烯的制备 | 试剂X | 试剂Y |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
C | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | Br2的CCl4 |
A.AB.BC.CD.D
【答案】A
【解析】
A、发生消去反应生成乙烯,乙醇与Br2的CCl4溶液不反应,乙烯与Br2的CCl4溶液反应,则不需要除杂,不影响乙烯检验,故A选;
B、发生消去反应生成乙烯,水吸收乙醇,乙醇能被高锰酸钾氧化,则需要加水除杂,否则干扰乙烯的检验,故B不选;
C、发生消去反应生成乙烯,NaOH溶液吸收乙醇,乙醇能被高锰酸钾氧化,则需要NaOH溶液除杂,否则干扰乙烯的检验,故C不选;
D、发生消去反应生成乙烯,乙醇与Br2的CCl4溶液不反应,但可能混有二氧化硫,二氧化硫、乙烯均与溴水发生反应,则需要除杂,否则可干扰乙烯检验,故D不选;
答案选A。

练习册系列答案
 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目